Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
КвасцыСтатьи и работы по химии / Железоаммонийные квасцы / Статьи и работы по химии / Железоаммонийные квасцы / Квасцы Квасцы
Квасцы — двойные соли, кристаллогидраты сульфатов трёх- и одновалентных металлов общей формулы M+2SO4·M3+2(SO4)3·24H2O (часто записывается как M+M3+(SO4)2·12H2O), где M+ — один из щелочных металлов (литий, натрий, калий, рубидий или цезий), а M3+ — один из трехвалентных металлов (обычно алюминий, хром или железо(III)). Ион аммония (NH4+) может также выступать в роли M+.
Квасцы могут быть получены смешением горячих эквимолярных водных растворов сульфатов соответствующих металлов, при охлаждении таких растворов из них кристаллизуются квасцы.
Двойными называют соли, образованные двумя разными катионами с одним и тем же анионом. Например, при упаривании водного раствора, содержащего 1 моль сульфата аммония (NH4)2SO4 и 1 моль сульфата железа(III) Fe2(SO4)3, выделяется не смесь этих солей, а однородные кристаллы «железоаммонийных квасцов» – аммония-железа (III) сульфата додекагидрата , имеющие характерную октаэдрическую форму:
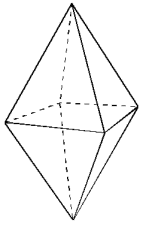
Двойные соли можно рассматривать как комплексные соединения, существующие только в кристаллическом состоянии. При растворении в воде они полностью распадаются на ионы. Так, квасцы диссоциируют на катионы аммония NH4+ и гексаакважелеза [Fe(Н2О)6]3+, сульфат-ионы SО42– и молекулы воды:
NH4Fe(SO4)2*12H2O = NH4+ + [Fe(Н2О)6]3+ + 2SO42– + 6H2O
Поэтому химическое поведение водных растворов двойных солей не отличается от поведения составляющих их обычных солей.
Квасцы хорошо растворяются в воде, их водные растворы имеют вяжущий кисловатый вкус и кислую реакцию из-за гидролиза, например:
[Аl(Н2О)6]3+ + Н2О ![]() [Аl(Н2О)5(ОН)]2+ + Н3О+.
[Аl(Н2О)5(ОН)]2+ + Н3О+.
При нагревании квасцы сначала плавятся в содержащейся в них воде, а затем эту воду теряют, образуя безводные соли. Дальнейшее нагревание превращает в смесь оксидов металлов.
Железоаммонийные квасцы - кристаллогидрат сульфата жезлеза-аммония NH4Fe(SO4)2 *12H2O .
Применяют в виде 0,5-1,0%-го водного раствора для полосканий, промываний и т.п. Благодаря тому, что соли трёхввалентных металлов вызывают денатурацию белков, их стали применять в медицине как вяжущее, прижигающее и кровеостанавливающее средство («квасцовый карандаш»).
Также квасцы используют для получения несгораемой бумаги, путем пропитывая проклеенной бумаги насыщенным водным раствором квасцов и высушивания ее потом на воздухе.
Квасцы применяют в приготовлении порошков и паст для очистки серебряных и золотых украшений, в которые также входят хлорид аммония (NH4Cl), ляпис (AgNO3), тиосульфат натрия (Na2S2O3), винный камень (гидротартарат калия); в приготовлении фотографических эмульсий на желатиновой основе; как дубящее средство в кожевенной промышленности; в качестве протравы при крашении шерстяных и хлопчатобумажных тканей; как коагулят при очистке воды; изготовлении огнестойких тканей; реагент для обнаружения SCN–, PO43–, AsO43– и др.
Смотрите также
Теория строения, многообразие, классификация и номенклатура
органических соединений. Типы химических реакций
Многообразие органических соединений, их свойств
и превращений объясняет теория химического строения (А. М. Бутлеров,
1861–1864).
Химическое строение – это определенная последовательность располо ...
Глюкоза
...


