Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Реакции обмена.Статьи и работы по химии / Выполнение лабораторных работ по химии в вузах / Гидролиз солей. / Статьи и работы по химии / Выполнение лабораторных работ по химии в вузах / Гидролиз солей. / Реакции обмена. Реакции обмена.
Обязательным условием течения реакций между электролитами является удаление из раствора тех или иных ионов - например, вследствие образования слабо диссоциирующих веществ, или веществ, выделяющихся из раствора в виде осадка или газа. Иначе говоря, реакции в растворах электролитов всегда идут в сторону образования наименее растворимых веществ.
Уравнения реакций в таких случаях рекомендуется записывать в молекулярно-ионной форме, которая позволяет лучше понять сущность протекающих процессов. В молекулярно-ионных уравнениях сильные электролит пишутся в виде ионов, а слабые электролиты, трудно растворимые вещества - в виде молекул.
Существует четыре случая обменных реакций в растворах электролитов, равновесие которых сильно смещено в сторону образования продуктов реакции:
1. Реакции, идущие с образованием осадка.
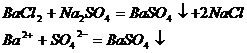
2. Реакции, сопровождающиеся образованием газообразных (летучих) веществ.
![]()
3. Реакции, протекающие с, образованием слабых электролитов.
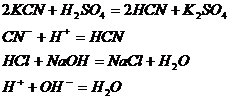
4. Реакции, идущие с образованием комплексных ионов.
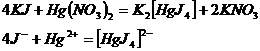
Смотрите также
Контрольные вопросы.
В чем
состоит главная задача химии?
Основанием
химии является основная двуединая проблема химии. В чем она заключается?
От
каких факторов зависят свойства вещества?
Запишите
четыре концеп ...
Нефть, ее свойства
Бурный научно-технический прогресс и высокие темпы развития
различных отраслей науки и мирового хозяйства в XIX – XX вв. привели к резкому
увеличению потребления различных полезных ископ ...


