Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Билет №16.Статьи и работы по химии / Билеты по химии 10 класс / Статьи и работы по химии / Билеты по химии 10 класс / Билет №16. Билет №16.
Основания, их классификация и химические свойства на основе представлений об электролитической диссоциации.
Основания — электролиты, при диссоциации которых образуется только один вид анионов — гидроксид-ионы.
![]()
Классификация оснований
1. Растворимые в воде (щелочи)— гидроксиды металлов главных подгрупп I и II групп.
![]()
2. Нерастворимые в воде
— гидроксиды остальных металлов.
![]()
Химические свойства
. Щелочи изменяют окраску индикаторов (лакмус становится синим, фенолфталеин – малиновым).
Взаимодействие с кислотами:
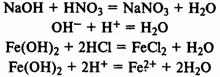
Взаимодействие с кислотными оксидами:
![]()
Растворы щелочей вступают в реакции ионного обмена с растворами солей, если образующийся при этом гидроксид нерастворим в воде:
![]()
При нагревании слабые основания разлагаются на оксиды металлов и воду:
![]()
Получение оснований.
Щелочи получают электролизом растворов солей.
Электролиз раствора хлорида натрия. Процессы на катоде и аноде:
![]()
Уравнение реакции:
![]()
Нерастворимые в воде основания получают реакцией обмена со щелочами:
![]()
Смотрите также
Одноосновные насыщенные карбоновые кислоты
...
Компьютерные технологии при изучении темы "Молекулярные перегруппировки"
В Государственной
программе развития образования России на 2005-2010 годы отмечается, что в
условиях быстроизменяющегося мира и увеличения потоков информации
фундаментальные предметные знан ...


