Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Лигандообменная хроматографияУчим химию / Учим химию / Лигандообменная хроматография Лигандообменная хроматография
Лигандообменная хроматография основана на образовании координационных связей между сорбентом и разделяемыми ионами или молекулами. Лигандообменная хроматография применима только для разделения соединений, содержащих донорные гетероатомы или кратные связи. Ионы переходных металлов, находящиеся в неподвижной фазе, являются акцепторами электронов и легко вступают в координационное взаимодействие с электронодонорными атомами функциональных групп разделяемого соединения. Для проведения лигандного разделения необходимо наличие склонных к координации органических соединений и комплексообразующего катиона металла. Такое разделение характеризуется обратимостью процесса и высокой скоростью обмена лигандов. Лигандный обмен применяют в жидкостной колоночной, тонкослойной и газовой хроматографии, но наибольшие успехи были достигнуты в ВЭЖХ.
Лигандообменную хроматографию применяют для разделения в водной среде соединений, представляющих большой интерес для органической химии и биохимии: аминов, аминокислот, белков, нуклеотидов, пептидов, углеводов. При этом в вчестве комплексообразующих используют ионы меди, цинка, кадмия, никеля, серебра и железа. Ионы ртути и серебра в неполярной среде алифатических углеводородов образуют лабильные комплексы с ненасыщенными и ароматическими углеводородами. Большими достоинствами лигандообменной хроматографии является ее селективность и отсутствие жестких требований к сорбенту, который может быть прочно связан ионами металла или только пропитан солями металла.
Аминокислоты занимают две координационные позиции, т.e. являются бидентатными лигандами, что резко повышает прочность их связывания за счет образования хелатного комплекса.
Лигандообменная хроматография оптически активных соединений основана на образовании лабильных координационных соединений, в которых с центральным ионом металла-комлексообразователя одновременно координирована молекула расщепляющего асимметрического реагента и один из подлежащих разделению энантиомеров. Для осуществления лигандообменной хроматографии необходимо наличие в расщепляющих реагентах и в разделяемых лигандах донорных гетероатомов серы, кислорода, азота, способных координироваться с ионом металла. Наблюдается хорошая координация α-аминокислот и ионов меди, цинка и никеля. Донорные атомы образуют плотно упакованную координационную сферу вокруг центрального иона металла, при этом разделяемые лиганды вступают в тесный контакт с расщепляющим реагентом. Этим и объясняется высокая эффективность распознавания реагента, т.e. энантиоселективность.
Такой принцип расщепления рацематов–лигандообменная хроматография – впервые был применен с использованием полистирольного сорбента, ковалентно связанного с остатками оптически активной природной аминокислоты L-пролина. Сорбент прочно координировал двухвалентную медь, оставляя в ее основной координационной плоскости две вакантные позиции для связывания подвижного лиганда молекулы L- или D-аминокислоты. Оказалось, что остаток L-пролина проявляет настолько высокое сродство к D-изомерам аминокислот, что последние пришлось даже вымывать из колонки раствором аммиака, который, координируясь с ионами меди, вытеснял подвижный лиганд из сорбционного комплекса, в то время как L-изомеры десорбировались водой.
Взаимодействием аминогруппы оптически активной аминокислоты с хлорметиль-ной группой полистирола в присутствии иодида натрия синтезировано более 50 сорбентов, имеющих асимметрические атомы. Оказалось, что циклические аминокислоты пролин и оксипролин обладают максимальной энантиоселективностью и количественно расщепляют рацематы практически всех аминокислот, а также многие оксикислоты,
диамины, аминоспирты. Достоинством полистирольных асимметрических сорбентов являются высокая химическая стабильность, большая обменная емкость и возможность препаративного расщепления рацематов. Иногда за один цикл на 300 г. сорбента удается расщепить до 20 г. рацемата. Появились лиган-дообменники с привитыми к сили-кагелю аминопропильным или полученным из него дитиокарбаматным радикалом.
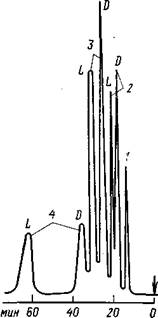
Рис. 1. Хроматограмма рацематов аминокислот, полученная на колонке размером 100Х1 мм (стекло) с асимметрическим полистирольным анионитом (7,5 мкм), подвижная фаза – 0,25 М ацетат натрия и 1,5Х10-3 М ацетат меди, рН=5,2, детектор–УФ (260 нм): 1 – лизин; 2 – аланин; 3 – серии; 4 – лейцин
Лигандообменную хроматографию с успехом применяют для производства оптически чистых меченных тритием аминокислот.
Весьма важное применение лигандообменной хроматографии – быстрое разделение асимметрических энантиомеров без предварительного отделения от сопутствующих примесей. В лигандообменной жидкостной хроматографии в отличие от лигандообменной газовой хроматографии не требуется предварительное превращение энантиомеров в легколетучие соединения. Обычно в качестве сорбента применяют полистирол, к которому привит радикал оптически активного бензилзамещенного пропилендиамина.
Для сокращения времени анализа, повышения его чувствительности и точности требуется повышение эффективности колонки, что достигается за счет уменьшения частиц полистирольного сорбента. Перспективным является получение сорбентов для лигандообменной хроматографии на основе пористых силикагелей, химически модифицированных активными лигандами. Поверхность силикагеля связывается через n-пропиленовые мостики с L-оксипролиновыми лигандами.
В настоящее время создано и испытано около десятка асимметрических силикагелевых сорбентов. Хотя в большинстве сорбентов использованы оптические изомеры пролина и оксипролина, они различаются сродством к различным аминокислотам и порядком их элюирования; это связано с тем, что подвижный лиганд фиксируется в комплексе не только координацией карбоксильной и аминогруппой с ионом меди, но и взаимодействием бокового радикала аминокислоты с ближайшим окружением координационного центра, что определяет в конечном итоге порядок удерживания антиподов аминокислот сорбенте.
Поскольку сорбенты для лигандообменной хроматографии выпускаются, предложены некоторые модификации метода, позволяющие использовать традиционные сорбенты. Так, N-алкилированные оптически активные аминокислоты сорбируются на обращенно-фазном силикагеле. В алкильном радикале должно быть больше 5–6 углеродных атомов. В этом случае модификатор прочно удерживается на сорбенте и не смывается водным элюентом, в который добавляют следовые количества меди.
Смотрите также
Оксираны (эпоксиды)
Оксиранами (старое
название эпоксиды) называют трехчленные циклические соединения, содержащие один
атом кислорода в цикле.
...
Мышьяк
Мышьяк (As)
Мышьяк (лат.
Arsenicum), As, химический элемент V группы периодической системы Менделеева, порядковый
номер 33, атомная масса 74,9216; кристаллы серо-стального цвета. Элемент
...
Исследование морфологической структуры, физико-химических и химических характеристик беленой, сульфатной целлюлозы из древесины хвойной породы
Одним
из наиболее важных факторов, определяющих развитие большинства отраслей
промышленности, является устойчивая сырьевая база, и в частности углерод
содержащее сырье. К такому сырью относ ...


