Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Химические
свойства радонаДипломы, курсовые и прочее / Радон, его влияние на человека / Дипломы, курсовые и прочее / Радон, его влияние на человека / Химические
свойства радона Химические
свойства радонаСтраница 1
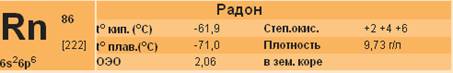
Ко времени открытия радона, типичного представителя благородных газов, существовало мнение, что элементы этой группы химически инертны и не способны образовывать истинные химические соединения. Известны были лишь клатраты, образование которых происходит за счет сил Ван-дер-Ваальса. К их числу относятся гидраты ксенона, криптона и аргона, которые получаются сжатием соответствующего газа над водой до давления, превышающего упругость диссоциации гидрата при данной температуре. Для получения аналогичных клатратов радона и обнаружения его по изменению упругости пара потребовалось бы практически недоступное количество этого элемента. Новый метод получения клатратных соединений благородных газов был предложен Б.А. Никитиным и состоял в изоморфном соосаждении молекулярного соединения радона с кристаллами специфического носителя. Изучая поведение радона при процессах соосаждения его с гидратами сернистого газа и сероводорода, Никитин показал, что существует гидрат радона, который изоморфно соосаждается с SO2Ч6H2O и H2SЧ6H2O. Масса радона в этих опытах составляла 10-11 г. Аналогично получены клатратные соединения радона с рядом органических соединений, например с толуолом и фенолом.
Исследования химии радона возможны лишь с субмикроколичествами этого элемента при использовании в качестве специфических носителей соединений ксенона. Следует, однако, учитывать, что между ксеноном и радоном находится 32 элемента (наряду с 5d-, 6s- и 6р-происходит заполнение 4f-орбит), что определяет большую металличность радона по сравнению с ксеноном.
Первое истинное соединение радона —дифторид радона — было получено в 1962 г. вскоре после синтеза первых фторидов ксенона. RnF2 образуется как при непосредственном взаимодействии газообразных радона и фтора при 400°С, так и при окислении его дифторидом криптона, ди- и тетрафторидами ксенона и некоторыми другими окислителями. Дифторид радона устойчив до 200° С и восстанавливается до элементарного радона водородом при 500°С и давлении H2, равном 20 МПа. Идентификация дифторида радона осуществлена путем изучения его сокристаллизации с фторидами и другими производными ксенона.
Ни с одним окислителей не получено соединение радона, где его степень окисления была бы выше +2. Причиной этого является большая устойчивость промежуточного продукта фторирования (RnF+X-) по сравнению с аналогичной формой ксенона. Это обусловлено большей ионностью связи в случае радонсодержащей частицы. Как показали дальнейшие исследования, преодолеть кинетический барьер реакций образования высших фторидов радона можно либо введением в реакционную систему дифторида никеля, обладающего наивысшей каталитической активностью в процессах фторирования ксенона, либо осуществлением реакции фторирования в присутствии бромида натрия. В последнем случае большая, чем у дифторида радона, фтордонорная способность фторида натрия позволяет конвертировать RnF+ в RnF2 в результате реакции: RnF+SbF6 + NaF = RnF2 + Na+SbF6. RnF2 фторируется с образованием высших фторидов, при гидролизе которых образуются высшие оксиды радона. Подтверждением образования соединений радона в высших валентных состояниях является эффективная сокристаллизация ксенатов и радонатов бария.
Долгое время не находили условий, при которых благородные газы могли бы вступать в химическое взаимодействие. Они не образовывали истинных химических соединений. Иными словами их валентность равнялась нулю. На этом основании было решено новую группу химических элементов считать нулевой. Малая химическая активность благородных газов объясняется жёсткой восьмиэлектронной конфигурацией внешнего электронного слоя. Поляризуемость атомов растёт с увеличением числа электронных слоёв. Следовательно, она должна увеличиваться при переходе от гелия к радону. В этом же направлении должна увеличиваться и реакционная способность благородных газов.Так, уже в 1924 году высказывалась идея, что некоторые соединения тяжелых инертных газов (в частности, фториды и хлориды ксенона) термодинамически вполне стабильны и могут существовать при обычных условиях. Через девять лет эту идею поддержали и развили известные теоретики — Полинг и Оддо. Изучение электронной структуры оболочек криптона и ксенона с позиций квантовой механики привело к заключению, что эти газы в состоянии образовывать устойчивые соединения с фтором. Нашлись и экспериментаторы, решившие проверить гипотезу, но шло время, ставились опыты, а фторид ксенона не получался. В результате почти все работы в этой области были прекращены, и мнение об абсолютной инертности благородных газов утвердилось окончательно.
Смотрите также
Производство аммиака: краткая характеристика
Общей экономической
задачей каждого химического предприятия является получение химических веществ высокого
качества и в достаточном количестве, чтобы их реализация приносила прибыль. С этим
...
Реакции фенолов
Фенолы могут реагировать как
по гидроксильной группе, так и по бензольному кольцу.
...
Углеводородный состав прямогонных бензинов
Бензин
(от франц. benzine) - смесь легких углеводородов с температурой кипения 30 –
205оС. Прозрачная жидкость плотностью 0,70-0,78 г/см3. Производится
путем смешивания компонентов первично ...


