Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Направленность ковалентной связи.Статьи и работы по химии / Атомно-молекулярное учение и его законы / Химическая связь и строение молекул. / Статьи и работы по химии / Атомно-молекулярное учение и его законы / Химическая связь и строение молекул. / Направленность ковалентной связи. Направленность ковалентной связи.Страница 1
Выше указывалось, что электронные орбитали (кроме s-орбиталей) имеют пространственную направленность. Поэтому ковалентная связь, являющаяся результатом перекрывания электронных облаков взаимодействующих атомов, располагается в определенном направлении по отношению к этим атомам. Если перекрывание электронных облаков происходит в направлении прямой, соединяющей ядра взаимодействующих атомов (т. е., по оси связи), то образуется s-связь (сигма-связь) (рис. 5).
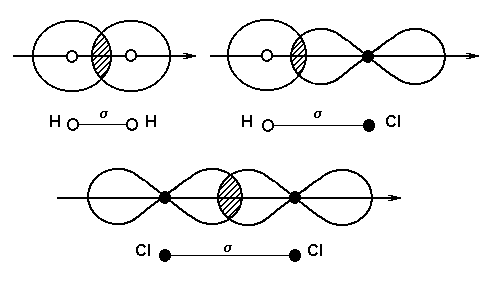
Рис. 5. Схематическое изображение сигма-связи в молекулах водорода, хлороводорода и хлора.
При взаимодействии p-электронных облаков, направленных перпендикулярно к оси связи, образуются две области перекрывания расположенные по обе стороны от этой оси. Такая ковалентная связь называется p-связью (пи-связь). p-Связь может возникнуть не только за счёт p-электронов, но также за счет перекрывания d- и p-электронных облаков (б) или d-облаков (в) (рис. 6).
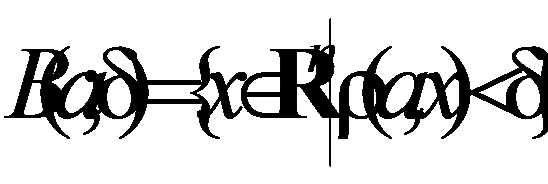
Рис. 6. Схематическое изображение p-связи.
Пользуясь представлением о направленности ковалентных связей, можно объяснить пространственное расположение атомов в некоторых молекулах. Например, в молекуле воды связь между атомами осуществляется двумя ковалентными связями, образующимися в результате перекрывания 1s-электронных облаков двух атомов водорода с электронными облаками двух неспаренных 2p-электронов атома кислорода (рис. 7). p-Электронные облака атома кислорода взаимно перпендикулярны, поэтому следует ожидать, что и молекула воды будет иметь угловое строение. Этот вывод подтверждается структурными исследованиями. Следует, однако, отметить, что угол между ковалентными связями составляет 104,5°, а не 90°, как можно было ожидать. Различие рассчитанных и экспериментально полученных величин валентных углов наблюдается и во многих других соединениях. Объяснением этого может служить гибридизация атомных орбиталей.
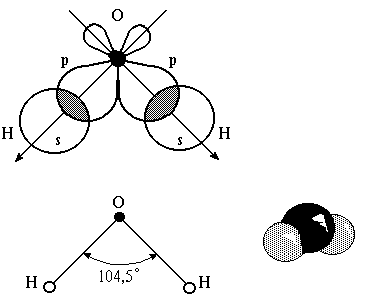
Рис. 7. Строение молекулы воды.
При образовании молекулы электронные облака изменяют свою форму. Например, вместо неравноценных s- и p-электронных облаков могут образовываться равноценные гибридные (смешанные) электронные облака. В результате гибридизации электронные облака приобретают более вытянутую форму. Это обеспечивает большее их перекрывание и, следовательно, увеличивает энергию ковалентной связи. Выигрыш энергии превышает затраты её на осуществление гибридизации электронных орбиталей. На рис. 8 показана форма гибридного sp-облака. Из s- и p-орбитали образуются две гибридные sp-орбитали, вытянутые в противоположных направлениях. В зависимости от числа и типа орбиталей, участвующих в гибридизации, взаимное расположение гибридных орбиталей в пространстве будет различным. Если в гибридизации принимают участие одна s- и две p-орбитали (sp2-гибридизация), то образуются три равноценные гибридные орбитали, располагающиеся в одной плоскости и ориентированные друг относительно друга под углом 120 ° (рис. 9).
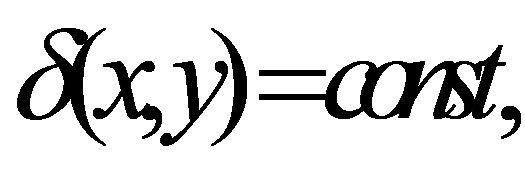
Рис. 8. Расположение электронных облаков при sp-гибридизации: а ¾ (s + p)-облака, б ¾ два sp-облака.
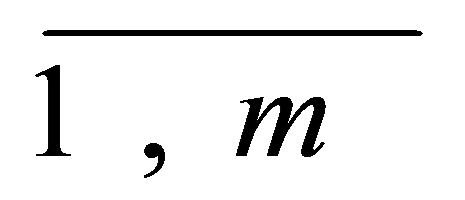
Рис. 9. Расположение электронных облаков при sp2-гибридизации: а ¾ (s + p + p)-облака, б ¾ три sp2-облака.
При гибридизации типа sp3, в которой принимает участие одна s- и три p-орбитали, образующиеся равноценные четыре орбитали вытянуты в направлениях к вершинам тетраэдра.
У атомов элементов III и последующих периодов, имеющих d-орбитали, в гибридизации часто принимают участие две d-, одна s- и три p-орбитали (sp3d2-гибридизация). В этом случае образуется шесть равноценных гибридных орбиталей, направленных к вершинам октаэдра.
Смотрите также
Ознакомление с некоторыми операциями
лабораторной практики и измерительными приборами.
Цель
работы - ознакомление студентов с взвешиванием, измерением объемов жидкостей,
титрованием и др., а также с некоторыми химическими и измерительными приборами.
При подготовке к
выполнению ла ...
Моделирование парожидкостного равновесия
Выбор модели, адекватно описывающей
фазовое равновесие системы, является важным и необходимым шагом при решении
массообменного процесса. На сегодняшний день разработано достаточно большое
число мет ...
Описание технологического процесса получения грунтовки водно-дисперсионной глубокого проникновения
...


