Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Образование пептидных связейДипломы, курсовые и прочее / Органическая химия / Дипломы, курсовые и прочее / Органическая химия / Образование пептидных связей Образование пептидных связей
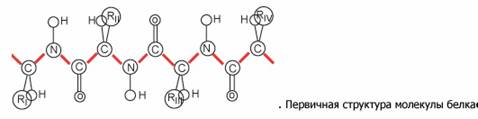
Первичная структура – последовательность соединения аминокислотных остатков в полипептидной цепи.

Вторичная структура – пространственная конфигурация, которую принимает полипептидная цепь. Поддерживается благодаря водородным связям между группами – СО- и –NH-, расположенными на соседних витках спирали.
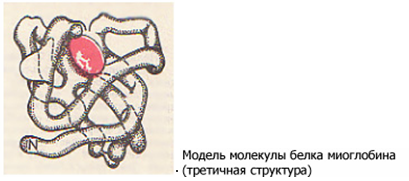
Третичная структура – это конфигурация, которую принимает в пространстве закрученная в спираль полипептидная цепь. Поддерживается взаимодействием между функциональными группами радикалов полипептидной цепи (-NH2, -OH, -COOH).
Существует и четвертичная структура белка. Важное свойство белков – способность подвергаться гидролизу:
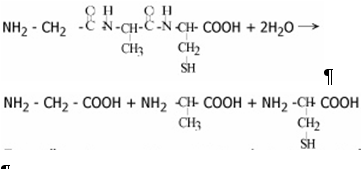
Под действием химическим веществ (кислот, щелочей, спиртов), при нагревании, действии радиации, солей тяжелых металлов происходит разрушение вторичной и третичной структур белка до первичной – денатурация.
Белки горят с характерным запахом жженых перьев. Для распознавания белков используют цветные реакции:
· ксантопротеиновую:
· раствор белка +HNO3 (конц.) ® желтое окрашивание;
· биуретовую:
· раствор белка +Cu(OH)2 ® красно-фиолетовое окрашивание;
Сложные белки:
· Фосфопротеины - входят в состав казеина молока.
· Гликопротеины - содержатся в плазме крови, слюне (муцин).
· Нуклеопротеины - входят в состав хромосом.
· Хромопротеины - входят в состав гемоглобина.
· Липопротеины - входят в состав мембран, транспортная система крови.
· Флавопротеины - компонент для переноса электронов при дыхании.
Смотрите также
Экспериментальная часть
Реагенты
и оборудование.
Уравнение
реакции имеет вид:
Реактивы:
N-фенилантраниловая кислота (С13Н11О2N, M=213 г/моль, Тпл=179-1810С) – 3г,
серная кислота (Н2SО4, M=98.08 г/моль, Тпл=-13 ...
Жесткость
Вода, в которой
растворены соли кальция и магния, обладает особым свойством – жесткостью.
Жесткость, обусловленная содержанием гидрокарбонатов кальция и магния,
называется карбонатной. Ее находят т ...


