Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Планетарная модель атома Резерфорда.Статьи и работы по химии / Атомно-молекулярное учение и его законы / Cтроение атома и периодический закон Д. И. Менделеева / Статьи и работы по химии / Атомно-молекулярное учение и его законы / Cтроение атома и периодический закон Д. И. Менделеева / Планетарная модель атома Резерфорда. Планетарная модель атома Резерфорда.Страница 1
Принимая во внимание изложенное выше, а также электронейтральность атома, следует заключить, что в нём должна находиться положительно заряженная составная часть, заряд которой уравновешивает отрицательные заряды электронов. Эта положительно заряжнная часть атома, открытая в 1911 г. английским физиком Э. Резерфордом, была названа ядром атома.
Резерфорд изучал траектории полёта a-частиц, бомбардирующих листки золотой фольги толщиной около 0,0005 мм. Учёный обнаружил, что подавляющее большинство a-частиц, пройдя через фольгу, продолжало двигаться в прежнем направлении. Небодьшая часть a-частиц отклонялась от своего пути на различные углы, а отдельные частицы начинали двигаться в противоположном направлении. Это явление известно под названием рассеяние a-частиц (рис. 4). Такое поведение a-частиц можно объяснить лишь тем, что они, проходя через металл, как бы наталкивались на положительно заряженную часть атома — ядро, масса которого больше массы a-частицы, и попадали в поле действия кулоновских сил отталкивания. (Столкновение с электроном не может существенно отразиться на траектории a-частицы, так как масса электрона (9,1·10-18 г) почти в 7500 раз меньше a-частицы.)
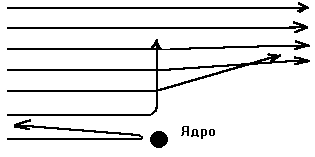
Рис. 4. Рассеяние a-частиц.
Проходя через фольгу, a-частицы встречают на своём пути множество атомов металла, но отклоняются от первоначального пути очень редко (отклоняется только одна из ста тысяч a-частиц, прошедших через фольгу). Это можно объяснить лишь тем, что размеры ядра очень малы по сравнению с размерами атома и вероятность того, что траектория полёта a-частицы пройдёт через ядро, очень мала. Основная масса a-частиц пролетает сквозь атом, не меняя направления движения.
Если предположить, что атом, ядро и электрон имеют форму шара, то диаметр атома будет равен примерно 10-8 см, а диаметр ядра — 10-13 см, т. е. ядро занимает примерно 1/1015 часть объёма атома. Если для наглядности представить себе атом увеличенным до размеров шара диаметром 100 м (высота тридцатиэтажного дома), то ядро атома в этом случае имело бы диаметр не более 1 мм. В то же время масса атома фактически сосредоточена в ядре. Следовательно, плотность атомных ядер очень велика. Если бы можно было собрать 1 см3 атомных ядер, то их масса оказалась бы равной приблизительно 116 млн. т.
Э. Резерфорд предложил планетарную модель атома, согласно которой ядро находится в центре атома, а электроны вращаются вокруг ядра подобно планетам, вращающимся вокруг Солнца. Заряды электронов уравновешиваются положительным зарядом ядра, и атом в целом остаётся электронейтральным. Возникающая вследствие вращения электронов центробежная сила уравновешивается электростатическим притяжением электронов к противоположно заряженному ядру.
Опыты по рассеянию a-частиц позволили не только установить существование атомного ядра, но и определить его заряд. Оказалось, что положительный заряд ядра атома численно равен порядковому номеру элемента в периодической сиситеме. Следовательно, порядковый номер элемента не просто регистрирует его положение в периодической системе, а является важнейшей константой элемента, выражающей положительный заряд ядра его атома. Из электронейтральности атома следует, что и количество вращающихся вокруг ядра электронов равно порядковому номеру элемента. Таков физический смысл порядкового номера элемента в Периодической системе элементов.
Создание Резерфордом планетарной, или ядерной, модели атома было крупным шагом вперёд в познании строения атома. Но в некоторых случаях эта теория вступала в противоречие с твёрдо установленными фактами.
Так, планетарная модель не могла объяснить устойчивости атома. Вращаясь вокруг ядра, электрон должен часть своей энергии испускать в виде электромагнитных колебаний, что должно привести к нарушению равновесия между электростатическим притяжением электрона к ядру и центробежной силой, обусловленной вращением электрона вокруг ядра. Для восстановления равновесия электрон должен переместиться ближе к ядру. Следовательно, непрерывно излучая электромагнитную энергию, электрон должен постепенно приближаться к ядру и в конце концов упасть на него — существование атома должно прекратиться. В действительности атом очень устойчив и может существовать бесконечно долго.
Модель Резерфорда не могла объяснить также характер атомного спектра. Известно, что солнечный свет, проходя через стеклянную призму, образует спектр — цветную полосу, содержащую все цвета радуги. Это явление объясняется тем, что солнечный свет состоит из электромагнитных волн различных частот. Волны различных частот неодинаково преломляются призмой, что приводит к образованию сплошного спектра. Аналогично ведёт себя свет, излучаемый раскалёнными жидкостями и твёрдыми телами. Спектр раскалённых газов и паров представляет собой отдельные цветные линии, разделённые тёмными промежутками, — линейчатый спектр. При этом атомы одного элемента дают вполне определённый спектр, отличающийся от спектра другого элемента. На рис. 5 показана видимая часть атомного спектра водорода.
Смотрите также
Изучение растворимости бензоата свинца в различных растворителях
Знание
растворимости какого-либо продукта изучаемого взаимодействия, в частности в нашем
случае бензоата свинца, имеет большое значение при решении различных практических
задач [1]. Наприме ...
Промышленная технология производства катализатора дегидрирования изоамиленов в изопрен марки КИМ-1
Одним из основных направлений
развития химической промышленности является создание мощного современного
производства пластических масс и каучуков. Особо важное значение приобретают
мономеры ...


