Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Гексацианоферраты(II, III)Дипломы, курсовые и прочее / Синтез и свойства комплексов железа (II) и железа (III) / Дипломы, курсовые и прочее / Синтез и свойства комплексов железа (II) и железа (III) / Гексацианоферраты(II, III) Гексацианоферраты(II, III)
Для железа (II) очень устойчивы цианидные комплексы (цианоферраты (II)). Наиболее известным из них является гексацианоферрат (II) калия — желтая кровяная соль.
Желтая кровяная соль (гексацианоферрат (II) калия — K4[Fe(CN)6]) известна с середины XVIII века. Первоначально ее получали сплавлением отходов скотобоен (например, крови животных, копыт, кож и т. п.) с поташем (К2СO3) и железными обрезками. После остывания расплава и выщелачивания его водой получали желтую кровяную соль.
Сейчас гексацианоферрат (II) калия получают, действуя избытком KCN на соли двухвалентного железа:
FeCl2 + 6KCN = K4[Fe(CN)6] + 2KC1.
При добавлении к раствору солей трехвалентного железа раствора желтой кровяной соли образуется темно-синий осадок, называемый берлинской или npyccкой лазурью [13]:
4FeCl3 + 3K4[Fe(CN)6] = FeIII4 [FeII(CN)6]3 + 12KCl.

Фото. 2. Берлинская лазурь
Это — качественная реакция на соли Fe3+.
Если на желтую кровяную соль подействовать окислителем (хлором, перманганатом калия), то получается комплексная соль трехвалентного железа гексацианоферрат (III) калия — K3[Fe(CN)6], которая окрашена в красный цвет и называется красной кровяной солью.
2K4[Fe(CN)6] + С12 = 2K3[Fe(CN)6] + 2KC1.

Фото. 1. Красная кровяная соль.
Красная кровяная соль (комплекс [Fe(CN)6]3-), менее устойчива, чем желтая (комплекс [Fe(CN6)]4-), и поэтому очень ядовита.
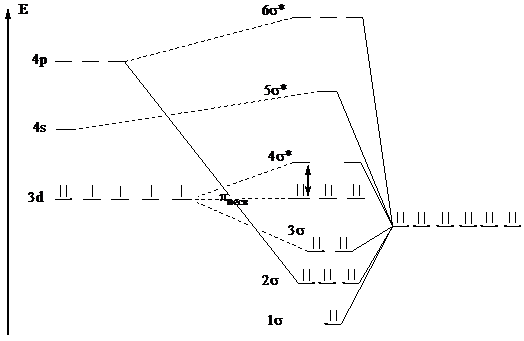
Рис. 5. Энергетическая диаграмма [Fe(CN6)]4- (метод МО).
При взаимодействии растворов солей двухвалентного железа с красной кровяной солью образуется темно-синий осадок, называемый турнбулевой синью:
3FeCl2 + 4K3[Fe(CN)6] = FeIII4 [FeII(CN)6]3 + 6KC1 + 6KCN.
Это — качественная реакция на соли Fe2+.
Ранее считалось, что при этом образуется гексацианоферрат (III) железа (II), то есть FeII3[Fe(CN)6]2, именно такую формулу предлагали для «турнбулевой сини». Теперь благодаря исследованиям по методу мессбауэровской спектроскопии известно, что турнбулева синь и берлинская лазурь — одно и то же вещество, а в процессе реакции происходит переход электронов от ионов Fe2+ к гексацианоферрат (III)- иону [6]:
Fe2+ + [Fe3+(CN)6]3- → Fe3+ + [Fe2+(CN)6]4-.
Этот процесс происходит практически мгновенно, а обратную реакцию можно осуществить лишь в вакууме при 300 0С [6]. Этот факт объясняется, по-видимому, тем, что комплекс [FeII(CN)6]4- более устойчив, чем [FeIII(CN)6]3-.
Турнбулева синь и берлинская лазурь плохо растворимы в воде, что затрудняет их использование в виде красок. Для повышения растворимости гексацианоферратов вводят ионы калия вплоть до состава KFe[Fe(CN)6] (последнее соединение называется растворимой берлинской лазурью). По мере увеличения содержания ионов калия цвет соединений меняется от темно- до светло-синего.
Схема структуры растворимой «берлинской лазури» – «турнбулевой сини» (кристаллогидрат вида KFeIII[FeII(CN)6]·H2O) приведена на рисунке 6 [6].
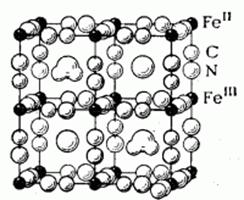
Рис. 6. Кристаллическая решетка «берлинской лазури»
Из неё видно, что атомы Fe2+ и Fe3+ располагаются в кристаллической решётке однотипно, однако по отношению к цианидным группам они неравноценны, преобладает тенденция к размещению Fe2+ между атомами углерода, Fe3+ - между атомами азота, ионы К+ и молекулы H2O располагаются в пустотах кристаллической решетки.
Хотя состав, структура и кристаллические решетки берлинской лазури и турнбулевой сини идентичны, различные исторические названия продолжают сохраняться, отражая химию ионов железа в различных степенях окисления.
Смотрите также
Анализ лекарственной формы состава: Rp.: Amidopyrini 0,3 Dibazoli 0,02
Амидопирин – белые кристаллы или белый кристаллический порошок без запаха,
слабогорького вкуса. Температура плавления 110 – 113 °С. Медленно растворяется в
воде, легко – в спирте и в хло ...
Свойства краун-эфиров и фуллеренов
Нанотехнология
и наноматериалы наряду с биотехнологией, информационными технологиями являются
ключевыми технологиями 21 века. Это подтверждается и резким ростом
финансирования данной отрасл ...
Изучение кето-енольной таутомерии на примере АУЭ
Цели работы
определены следующим образом:
1.
Изучить строение и свойства, а так
же особенности с ...


