Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Способы выражения концентрации растворовДипломы, курсовые и прочее / О растворах / Дипломы, курсовые и прочее / О растворах / Способы выражения концентрации растворов Способы выражения концентрации растворов
Концентрация является важной характеристикой раствора. Концентрация определяет относительное содержание компонентов в растворе.
Массовая доля
равна отношению массы растворённого вещества к массе раствора:
![]()
Молярная концентрация
– это количество вещества, содержащееся в одном литре раствора (моль/л):
![]()
![]()
Молярная концентрация эквивалента
(нормальная концентрация) – это число молей эквивалентов вещества, содержащихся в одном литре раствора (моль/л):
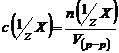 , где
, где
![]() - количество вещества эквивалента (моль);
- количество вещества эквивалента (моль);
![]() - фактор эквивалентности;
- фактор эквивалентности;
V(р-ра) – объём раствора (л).
Эквивалент – это реальная или условная частица вещества, которая в кислотно-основной реакции эквивалентна одному иону водорода, а в окислительно-восстановительной эквивалентна одному электрону.
Фактор эквивалентности ![]()
![]() – число, обозначающее, какая доля реальной частицы вещества Х эквивалентна одному иону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции.
– число, обозначающее, какая доля реальной частицы вещества Х эквивалентна одному иону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции.
Фактор эквивалентности рассчитывают на основе стехиометрии данной реакции из равенства
![]()
где z – основность кислоты или кислотность основания данной кислотно-основной реакции, а также число электронов, присоединяемых или теряемых частицей в данной окислительно-восстановительной реакции.
Молярной массой эквивалента вещества Х называют величину, измеряемую произведением фактора эквивалентности на молярную массу вещества Х
![]()
где ![]() - молярная масса эквивалента.
- молярная масса эквивалента.
Молярная масса эквивалента вещества – это масса одного моль эквивалентов. В разных реакциях одно и тоже вещество может иметь разные эквиваленты.
Моляльная концентрация
– это количество вещества, содержащееся в одном килограмме растворителя (моль/кг):
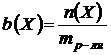
Молярная доля
равна отношению количества растворённого вещества к общему количеству веществ в растворе:
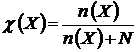
Как правило, вещество обладает определённой растворимостью в данном растворителе. Под растворимостью понимают концентрацию вещества в насыщенном растворе.
Раствор, находящийся в равновесии с растворяющимся веществом, называется насыщенным раствором.
Насыщенный раствор может как угодно долго находиться в равновесии с избытком растворяемого вещества (ΔGр−ния = 0), и его концентрация имеет максимально возможное в данных условиях значение.
Смотрите также
Термоэластопласты
Термопластичные эластомеры
(thermoplastic elastomers) – полимерные материалы, которые в
условиях эксплуатации способны, подобно эластомерам, к большим обратимым
деформациям, а при повышенных темпер ...
Методы анализа растворов и солей
...
Физико-химические методы исследования бетонных образцов
С
28 июня по 24 июля 2010 года я проходил практику в Дальневосточном научно - исследовательском
институте строительных материалов Российской академии архитектуры и
строительства Центре &quo ...


