Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Водородный показатель pHОткрытая химия / Растворы / Открытая химия / Растворы / Водородный показатель pH Водородный показатель pH
Для определения кислотно-основных свойств раствора пользуются водородным показателем pH. По определению, это отрицательный десятичный логарифм концентрации водородных ионов: pH = –lg [H+].
|
|
|
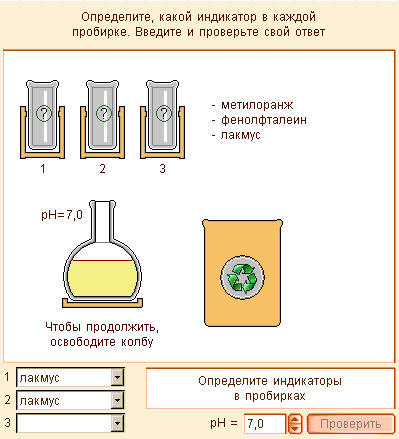
Модель 6.7. Индикаторы |
Очевидно, –lg [H+][OH–] = –lg 1 ∙ 10–14 дает pH + pOH = 14.
Тогда pH < 7 указывает на кислую среду, pH > 7 соответствует щелочной среде, pH = 7 – нейтральной среде.
Поскольку pH + pOH = 14, можно видеть, что pH может меняться от небольших отрицательных значений до величин, немного превышающих 14 (pH NaOH c C = 2 равен 14,3). На рис. 6.5 приведены pH некоторых бытовых растворов и пищевых продуктов.
 |
|
Рисунок 6.5 pH различных веществ и систем |
Смотрите также
Адсорбция
Адсорбция (от лат. ad — на, при и sorbeo — поглощаю), поглощение к.-л. вещества
из газообразной среды или раствора поверхностным слоем жидкости или твёрдого
тела. Например, если поместить в ...
Определение хлоридов в сточных водах
...
Выводы.
1. Отработана методика получения безводного
трихлорида самария.
2. Изучен механизм электровосстановления
иона самария в хлоридных и хлоридно-фторидных расплавах.
3. Показано, что для ...