Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Общие сведения о фосфорной кислотеУчим химию / Производство экстракционной фосфорной кислоты / Учим химию / Производство экстракционной фосфорной кислоты / Общие сведения о фосфорной кислоте Общие сведения о фосфорной кислоте
Кислота (ортофосфорная кислота) H3PO4, молярная масса 97,995; бесцветные гигроскопичные кристаллы моноклинной сингонии (а = 0,5762 нм, b = 0,4831 нм, с =1,1569 нм, ![]() = 95,31°, пространств, гр. Р21/с); расплывается на воздухе; т. пл. 42,50 С; плотность 1,88 г/см3;
= 95,31°, пространств, гр. Р21/с); расплывается на воздухе; т. пл. 42,50 С; плотность 1,88 г/см3; ![]() -1283 кДж/моль; наиболее стабильное соединение в ряду кислородсодержащих кислот фосфора. В расплавленном состоянии склонна к переохлаждению; при 15 0C образует густую маслянистую жидкость, при -121 0C- стеклообразную массу.
-1283 кДж/моль; наиболее стабильное соединение в ряду кислородсодержащих кислот фосфора. В расплавленном состоянии склонна к переохлаждению; при 15 0C образует густую маслянистую жидкость, при -121 0C- стеклообразную массу.
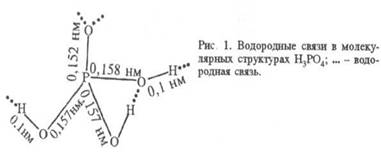
Фосфорная кислота смешивается с водой в любых соотношениях. Разбавленные водные растворы имеют кисловатый вкус. Из высококонцентрированных растворов кристаллизуется в виде гемигидрата (полугидрата) H3PO4·0,5H2O- бесцветные кристаллы моноклинной сингонии (а = 0,7922 нм, b = 1,2987 нм, с = 0,7470 нм, ![]() = 109,9°; пространств, гр. Р21/a). Молекула безводной H3PO4 и ее кристаллогидрата содержит тетраэдрическую группу PO4. В безводной фосфорная кислота образуются водородные связи типа P — О — H . O = P (рис. 1) (расстояние между атомами О 0,253 нм), которые удерживают структуры PO4 в виде слоев, параллельных одной из плоскостей кристалла. Водородные связи сохраняются и в концентрированных (70-80%) растворах фосфорная кислота, что отчасти обусловливает ее сиропообразную природу. В разбавленных до 40-50% растворах отмечена более устойчивая водородная связь фосфат-анионов с молекулами воды, а не с другими фосфат-анионами. В растворах фосфорная кислота имеет место обмен атомами кислорода между группами PO4 и водой.
= 109,9°; пространств, гр. Р21/a). Молекула безводной H3PO4 и ее кристаллогидрата содержит тетраэдрическую группу PO4. В безводной фосфорная кислота образуются водородные связи типа P — О — H . O = P (рис. 1) (расстояние между атомами О 0,253 нм), которые удерживают структуры PO4 в виде слоев, параллельных одной из плоскостей кристалла. Водородные связи сохраняются и в концентрированных (70-80%) растворах фосфорная кислота, что отчасти обусловливает ее сиропообразную природу. В разбавленных до 40-50% растворах отмечена более устойчивая водородная связь фосфат-анионов с молекулами воды, а не с другими фосфат-анионами. В растворах фосфорная кислота имеет место обмен атомами кислорода между группами PO4 и водой.
H3PO4 - сильная кислота, K1 7,1·10-3 (рКа 2,12), K2 6,2·10-8 (рКа 7,20), K3 5,0·10-13 (рКа 12,32); значения K1 и K2 зависят от температуры. Диссоциация по первой ступени экзотермична, по второй и третьей - эндотермична. В таблице приведены свойства растворов фосфорной кислоты
Фосфорная кислота при нормальных условиях малоактивна и реагирует лишь с карбонатами, гидроксидами и некоторыми металлами. При этом образуются одно-, двух- и трехзамещенные фосфаты. При нагревании выше 80 0C реагирует даже с неактивными оксидами, кремнеземом и силикатами. При повышенных температурах фосфорная кислота- слабый окислитель для металлов. При действии на металлическую поверхность раствором фосфорной кислоты с добавками Zn или Mn образуется защитная пленка (фосфатирование). Фосфорная кислота при нагревании теряет воду с образованием последовательно пиро- и метафосфорных кислот:
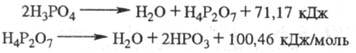
Фосфолеум (жидкий фосфорный ангидрид, суперфосфорная кислота) включает кислоты, содержащие от 72,4 до 88,6% P2O5, и представляет собой равновесную систему, состоящую из орто-, пиро-, Триполи-, тетраполи- и др. фосфорных кислот. При разбавлении суперфосфорной кислоты водой выделяется значит. кол-во тепла, и полифосфорные кислоты быстро переходят в ортофосфорную.
От других фосфорных кислот H3PO4 можно отличить по реакции с AgNO3 - выпадает желтый осадок Ag3PO4. Остальные фосфорные кислоты образуют белые осадки [1,5].
Смотрите также
Адсорбенты и ионные обменники в процессах очистки природных и сточных вод
...
Выделение жирных кислот из растительных масел
...
Свойства d-элементов 4-го периода.
Цель
работы - изучение химических свойств некоторых переходных металлов и их
соединений.
Металлы
побочных подгрупп, так называемые переходные элементы относятся к d - элементам,
поскольку в их ...


