Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Методы определения редуцирующих
веществ в гидролизатахУчим химию / Легко- и трудногидролизуемые полисахариды / Учим химию / Легко- и трудногидролизуемые полисахариды / Методы определения редуцирующих
веществ в гидролизатах Методы определения редуцирующих
веществ в гидролизатахСтраница 1
Для определения общего количества легко - или трудногидролизуемых полисахаридов находят концентрацию редуцирующих веществ в гидролизатах. Определение легко - и трудногидролизуемых полисахаридов по концентрации редуцирующих веществ не является вполне точным. В гидролизатах редуцирующими веществами будут не только моносахариды, но также и продукты их распада в кислой среде. В гидролизатах трудногидролизуемых полисахаридов PB состоят главным образом из глюкозы и небольших количеств маннозы, ксилозы, фруктозы. В гидролизатах легкогидролизуемых полисахаридов состав PB более разнообразен: глюкоза, манноза, галактоза, ксилоза, арабиноза, рамноза, глюкуроновая и галактуроновая кислоты, продукты распада моносахаридов. Все вещества имеют различную редуцирующую способность. Учесть эти различия при расчете результатов анализа практически невозможно. Поэтому принято концентрацию PB в гидролизатах определять чаще всего в пересчете на глюкозу. Для определения общего выхода PB пользуются методом Бертрана или эбулиостатическим методом, основанными на реакции окисления Сахаров медно-щелочным раствором, в результате которой двухвалентная медь Cu2+ переходит в одновалентную Cu+ и выпадает в осадок в виде оксида меди Cu2O. В качестве медно-щелочного раствора используют реактив Фелинга, который получают непосредственно при проведении анализа смешиванием растворов сульфата меди и щелочного раствора сегнетовой соли, в результате чего получается растворимый комплекс, содержащий Cu2+,
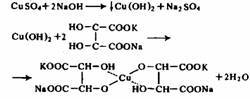
Упрощенно окисление альдоз реактивом Фелинга можно представить схемой
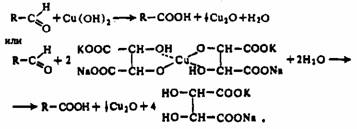
В действительности же окисление редуцирующих Сахаров медно-щелочным раствором представляет не одну определенную реакцию, а множество реакций, происходящих одновременно. При этом носителями редуцирующих свойств являются не только сами сахара, но и продукты их дальнейших превращений и распада. Таким образом, здесь нельзя ожидать стехиометрически протекающей реакции и написать точное уравнение реакции фактически невозможно. Поэтому для пересчета массы восстановленной меди в массу Сахаров пользуются эмпирическими таблицами.
Первоначально при определении PB методом Бертрана осадок Cu2O взвешивали. Впоследствии количество восстановленной меди стали определять титриметрическими методами - прямого или обратного титрования.
В прямом методе осадок Cu2O растворяют в растворе додекагидрата сульфата железа - аммония NH4Fe2 · 12Н20 в присутствии серной кислоты. При этом Cu+ окисляется в Cu2+, a Fe3+ восстанавливается в Fe2+ по уравнению
![]()
Раствор FeSO4 титруют раствором перманганата калия
![]()
По количеству перманганата калия, израсходованного на реакцию окисления железа, вычисляют массу меди в Cu2O и по эмпирической таблице находят массу Сахаров в пересчете на глюкозу.
Ввиду того, что оксид меди легко окисляется на воздухе, определение Сахаров приводит к неточным результатам. Кроме того, для метода Бертрана характерно большое число операций. При нагревании медно-щелочного раствора возможно его самовосстановление. Самовосстановление меди можно учесть, если провести контрольное определение.
Более точный и простой метод обратного титрования был разработан Макэном и Шоорлем. Этот метод основан на йодометрическом определении избытка реактива Фелинга.
![]() "
"
Смотрите также
Выводы
Таким
образом, в данной работе рассмотрен акридон, его свойства, способы получения и
применение. Приведены различные механизмы получения гетероциклических
соединений реакциями конденсации. Предложе ...
Свойства элементов подгруппы VIIIB.
Цель работы: изучение
химических свойств железа, кобальта, никеля.
Первую триаду VIIIВ группы
периодической системы, состоящую из Fе, Со, Ni, очень часто называют
семейством железа. На внешнем э ...


