Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Контактное окисление и адгезия к стали полиэтиленовых покрытийУчим химию / Учим химию / Контактное окисление и адгезия к стали полиэтиленовых покрытий Контактное окисление и адгезия к стали полиэтиленовых покрытийСтраница 1
Ранее [1,2] было установлено, что адгезия ПЭ-покрытий, окисляющихся на каталитически неактивной подложке, является функцией не только температуры Т и времени окисления т, но и толщины покрытий h. Уменьшение адгезии, характеризуемой удельным сопротивлением отслаиванию покрытий f при увеличении т обусловлено в основном проникновением к подложке низкомолекулярных продуктов термоокислительной деструкции макромолекул наружного поверхностного слоя покрытий. При повышении Т существенную роль в снижении величины f играет также уменьшение степени окисления граничащего с подложкой слоя полимера, связанное с ускорением процесса окисления в поверхностном слое покрытий.
Окисление граничащего с подложкой слоя осуществляется в основном кислородом, диффундирующим в покрытие из окружающей среды [3,4], а в катализе окисления полиолефинов на металлах существенную роль играют металлосодержащие продукты контактных реакций окисляющегося полимера с металлом, диффундирующие в покрытие (в основном соли карбоновых кислот) [5—7]. Поэтому следует ожидать, что закономерности изменения величины f для покрытий на каталитически активной подложке могут быть иными, чем на каталитически неактивной.
Цель данной работы — изучение адгезии ПЭ-покрытий толщиной 100—4000 мкм, окисленных на каталитически активной подложке (стали) [4,8,9] при различных температурно-временных условиях в среде воздуха: Г=433-453К, т=0,03-10,8 кс.
На рис. 1 представлены данные по влиянию т при различных температурах окисления на величину f для покрытий различной толщины на стали. Зависимость f от т при постоянных h и Т описывается кривой с максимумом. При увеличении h покрытий значение т, соответствующее максимуму f на изотермической кривой, сначала уменьшается, а затем увеличивается (рис. 1; рис. 2, б, кривая 4), в то время как для покрытий на каталитически неактивной подложке (алюминий [5]) оно только увеличивается [1]. Вследствие этого зависимость величины f покрытий на стали от h для постоянных Т и τ описывается при малых значениях τ кривой с максимумом, при средних т кривой с двумя максимумами, при больших т кривой с максимумом (рис. 3, а, кривые 1—3).
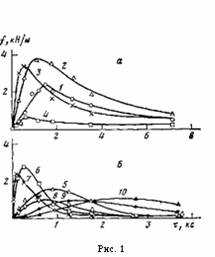
Рис. 1. Зависимость сопротивления отслаиванию ПЭ-покрытий на стали от времени их окисления т при 433 (а) и 453 К (б). Толщина покрытий 200 (1), 300 (5), 500 (2, 6), 800 (3, 7), 1000 (4, 8), 2000 (9) и 3000 мкм (10)
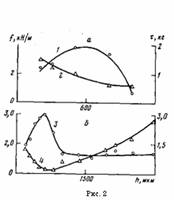
Рис. 2. Влияние толщины h ПЭ-покрытий на максимальные значения / (1, 3) для покрытий, окисленных при 433 (а) и 453 К (б), и время (2, 4), необходимое для достижения максимальной величины при 433 (а) и 453 К (б)
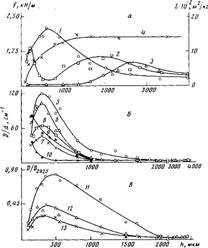
Рис. 3. Влияние толщины ПЭ-покрытий на стали, окисленных при 453 К в течение 0,6 (1), 1,2 (2, 10), 2,7 (S, 9) и 3,6 кс (3, 4, 5-7, 11-13), на сопротивление отслаиванию f (1—3), на площадь пика плавления S (4) (а), на накопление в граничащем со сталью слое солей карбоновых кислот (5, 8, 11), карбонильных (6, 9, 10, 12) и эфирных групп (7, 13) (б, в); б - данные, полученные методом ИК-спектроскопии пропускания для граничащего слоя толщиной 10 мкм; в — данные, полученные методом многократного нарушенного полного внутреннего отражения. Здесь и на рис. 5: D — оптическая плотность, d — эффективная толщина поглощающего слоя
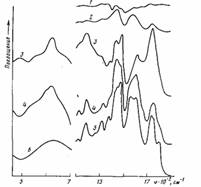
Рис. 4. ИК-спектры пропускания (1, 5) граничащего со сталью ело» толщиной 10 мкм (5) и остатков полимера на стали (1), а также ИК' спектры многократного нарушенного полного внутреннего отражения (2—4, 6) поверхности окисленной стали (6), стали, отслоенной от ПЭ-покрытия (2), и поверхности покрытия, контактировавшего со сталью, до (4) и после обработки в течение 7,2 кс раствором серной кислоты (3). Толщина покрытия 300 (1) и 500 мкм (2-5); время окисления при 453 К 0,6 (1); 1,8 (2); 3,6 кс (3-5)
Смотрите также
Термогравиметрия
Метод термического
анализа, основанный на непрерывной регистрации изменения массы (взвешивании)
образца в зависимости от его температуры в условиях программированного
изменения температуры среды. П ...
Пиррол
Пиррольное кольцо входит в структуру
многих важных природных соединений, таких как гемин, хлорофил и др. ...


