Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Последовательные реакцииОткрытая химия / Химическая кинетика / Открытая химия / Химическая кинетика / Последовательные реакции Последовательные реакции
Последовательными называют реакции с промежуточными стадиями, когда продукт предыдущей стадии служит исходным веществом для последующей:
| |
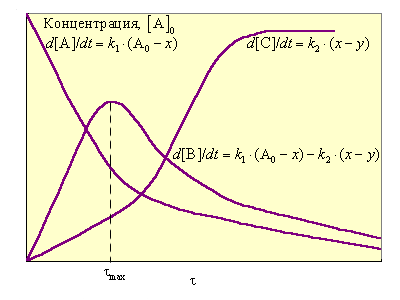
Зависимость концентраций реагентов этой двустадийной реакции приведена на рис. 5.6.
 |
|
Рисунок 5.6 Изменение концентраций A, B и С для последовательной реакции A → B → C; x – концентрация A0, превратившегося в В, y – концентрация образовавшегося С |
При k1 >> k2 все исходное вещество может превратиться в промежуточный продукт В, прежде чем начнется вторая реакция. Скорость всей реакции определяется второй стадией. При k1 << k2 концентрация промежуточного продукта мала, поскольку он не успевает накапливаться; эта стадия определяет скорость реакции в целом. Таким образом, скорость определяется самой медленной стадией (принцип лимитирующей стадии).
Смотрите также
Алифатические амины
Амины - производные аммиака, в которых атомы водорода замещены на
углеводородные радикалы. Амины классифицируют по числу атомов водорода,
замещенных на углеводородные радикалы. Различают первичные R ...
Ультрафиолетовое отверждение лаков и красок
На сегодняшний
момент в различных областях науки и промышленности ведутся активные
исследования, направленные на создание ресурсо- и энергосберегающих
экологически безопасных технологий. В ...


