Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Проведение анализаУчим химию / Химический анализ электролита ванн хлорирования на машиностроительном заводе / Учим химию / Химический анализ электролита ванн хлорирования на машиностроительном заводе / Проведение анализа Проведение анализаСтраница 1
В мерную колбу вместимостью 10 см3 отбирают 5см3 электролита, доливают водой до метки и перемешивают. В коническую колбу вместимостью 500см3 отбирают 5см3 полученного раствора, приливают 20см3 H2SO4 из бюретки 50см3 0,1н раствора соли Мюра, приливают 150-200см3 воды и титруют 0,1н раствором калия марганцевокислого до перехода окраски от зеленовато-голубого в слабо-розовую.
Параллельно устанавливают соотношение между 0,1н растворами калия марганцевокислого и соли Мюра. Для этого в коническую колбу вместимостью 500см3 приливают 20см3 H2SO4 из бюретки 50см3 соли Мюра, 200-250см3 воды и титруют 0,1н раствором марганцевокислого калия до слабо-розовой окраски.
Расчет
![]()
где V1 – объем 0,1н раствора соли Мюра, прилитый к пробе, см3;
е – соотношение между0,1н растворами марганцевокислого калия и соли Мюра;
V2 – объем 0,1н раствора марганцевокислого калия, израсходованного на титрование избытка соли Мюра, см3;
0,00333 – титр 0,1н раствора перманганата калия;
k – коэффициент поправки на титр 0,1н раствора перманганата калия;
V – объем электролита, взятый на анализ, см3.
Определение серной кислоты
Весовой метод
Сущность метода. Метод основан на осаждении серной кислоты раствором хлористого бария в виде сернокислого бария: H2SO4+BaCl4 → BaSO4+2HCl
Шестивалентный хром предварительно восстанавливают до трехвалентного перекисью водорода в присутствии соляной кислоты:
K2Cr2O7+H2O2+8HCl → 2CrCl3+2Cl+5H2O+2O2
Осадок сернокислого бария отделяют прокаливанием и взвешивают.
Барий хлористый раствор 10%
Кислота соляная раствор 1:1
Кислота уксусная
Перекись водорода
Проведение анализа
В коническую колбу вместимостью 250см3 отбирают 10см3 электролита, разбавляют водой до объема 100-150см3 приливают 20см3 разбавленной 1:1, добавляют по каплям пергидроль до окончания образования пузырьков. Раствор кипятят 15 минут. Приливают 10мл уксусной кислоты и нагревают до кипения.
В горячий раствор прибавляют по каплям при перемешивании 15см3 горячего раствора хлористого бария и кипятят 5 минут.
Раствор выдерживают в теплом месте 4-6ч, после чего фильтруют через плотный бузольный фильтр. Осадок промывают горячей водой до удаления ионов хлора. Промытый фильтр с осадком помещают в тигель, сушат, прокаливают до постоянного веса при температуре (800-900ºС).
Охлаждают в эксикаторе, взвешивают.
Расчет
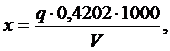
где q – масса осадка сернокислого бария, г;
0,4202 – коэффициент пересчета с сернокислого бария на серную кслоту;
V – объем электролита, взятый на анализ, см3.
Определение окиси хрома
Объемный перманганатометрический метод
Сущность метода. Метод основан на окислении трехвалентного хрома подсернокислым аммонием до шестивалентного по реакции:
Cr2(SO4)3+2(NH4) 2S2O8+7H2O → H2Cr2O7+3(NH4) 2SO4+6H2SO4
Содержание трехвалентного хрома вычисляют по разности между общим и шестивалентным хромом.
Реактивы и растворы
Аммоний подсернокислый, 12% раствор
Соль Мора, 0,1н раствор
Калий марганцевокислый, 0,1н раствор
Кислота серная, разбавленная 1:5
Натрий хлористый раствор 5%
Серебро азотнокислая 1% раствор.
Проведение анализа
В мерную колбу емкостью 100см3 5см3 электролита доливают водой до метки. В коническую колбу на 500см3 помещают 5см3 раствора, приливают 100см3 воды, 15см3 серной кислоты разбавленной 1:5, 5см3 1%-ного раствора нитрата серебра, 20см3 12%-ного раствора аммония подсернокислого и кипятят 3-5 минут до появления малиновой окраски. Затем добавляют 5см3 раствора хлористого натрия и кипятят до перехода окраски раствора в желтую и коагуляции осадка хлористого серебра.
Смотрите также
Формулы веществ-составление
Предлагаемое учебное пособие
содержит материал необходимый для полноценного обучения основам общей химии. В
книге приведены правила общей химии, которые подробно разобраны на конкретных
при ...
Физико-химические методы анализа веществ
В практической
деятельности часто возникает необходимость идентификации (обнаружения) того или
иного вещества, а также количественной оценки (измерения) его содержания.
Химическая
иденти ...
Фуллерены
Для химика, основные области интересов
которого - изучение превращений известных веществ и синтез новых, элементарный
углерод - не самое интересное из веществ. Ситуация замечательным образом ...


