Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Механизм реакции SNУчим химию / Функциональные замещенные алициклических и ароматических соединений / Учим химию / Функциональные замещенные алициклических и ароматических соединений / Механизм реакции SN Механизм реакции SNСтраница 1
Существует два основных типа реакций ионного замещения алифатических соединений: SN2 и SN1.
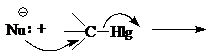
Нуклеофилом называется атом (или частица), который может отдать пару электронов любому элементу, иному чем водород. Hlg, который вытесняется (замещается) уходящей группой.
Реакция SN2
Энергетический профиль SN2-замещения
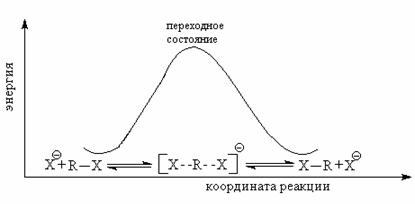
Частичное связывание между нуклеофилом, уходящей группой и атакуемым атомом обозначается пунктирной линией. Вцелом реакция проходит с обращением относительной конфигурации, это обращение называется вальденовским (Вальден, 1893).
В реакции принимают участие 2 частицы и скорость реакции определяется концентрацией как галоид алкила так и нуклеофила.
Влияние алкильных заместителей на скорость реакции.
По сравнению с другими гидридными состояниями углерода реакции SN2 наиболее легко протекают у sp3-гибридизованного атома.
|
Алкильная группа |
Относительная скорость замещения |
|
|
30 |
|
|
1 |
|
|
0,03 |
|
|
0 |
Влияние растворителя
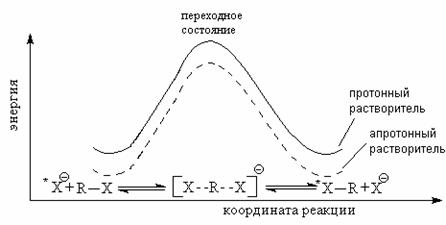
При увеличении полярности растворителя исходное соединение стабилизируется в большей степени, чем активированный комплекс, а стало быть, и энергия активации.
Порядок реакционноспособности нуклеофилов в протонных растворителях следующий:
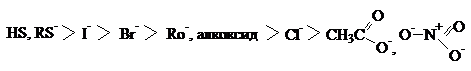
Ряд нуклеофильности галогенов:
![]()
Ряд уменьшения способности быть уходящей группой:
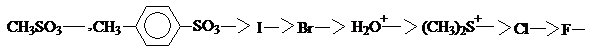
Реакция SN1
Характерна для третичных и вторичных алкилгалогенидов. SN1-реакция не является согласованным процессом и состоит из двух отдельных стадий:
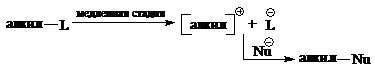
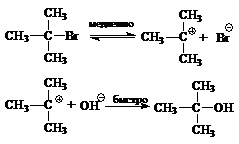
Скорость реакции зависит от концентрации бромистого алкила.
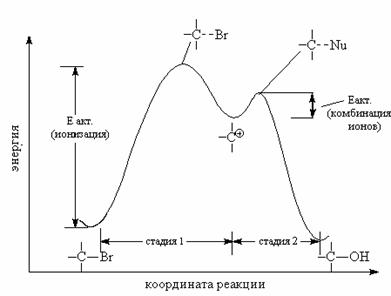
О стабильности карбкатионов, с которыми уже встречались при дегидратации спиртов:
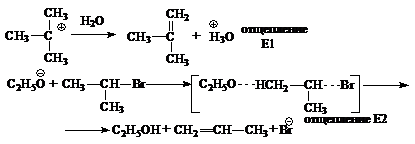
Действие хлора на углеродсодержащие вещества уже давно привлекало внимание многих химиков. Известно, что еще в 1815 г. Гей-Люсссак, обработав цианистоводородную кислоту хлором, обнаружил, что она превращается в хлорциан ![]() . Позже он же обратил внимание на то, что при отбеливании воска хлором последний поглощается воском, который при этом теряет равный хлору объем водорода.
. Позже он же обратил внимание на то, что при отбеливании воска хлором последний поглощается воском, который при этом теряет равный хлору объем водорода.
В 1821 г. Фарадеем было показано, что масло голландских химиков (дихлорэтан) при продолжительном действии на него хлора превращается в новый продукт — шестихлористый углерод ![]() , известный в настоящее время под названием гексахлорэтана. В этом случае было также обращено внимание на замену водорода равным объемом хлора.
, известный в настоящее время под названием гексахлорэтана. В этом случае было также обращено внимание на замену водорода равным объемом хлора.
Исследуя бензольные соединения, Велер и Либих (1822 г.) установили, что хлор превращает соединение ![]() , называвшееся в то время гидридом бензоила в хлористый бензоил:
, называвшееся в то время гидридом бензоила в хлористый бензоил: ![]() , с замещением одного атома водорода хлором и выделением эквивалентного количества хлористого водород.
, с замещением одного атома водорода хлором и выделением эквивалентного количества хлористого водород.
Смотрите также
Риформинг как способ получения бензинов с улучшенными характеристиками
Бензины являются
одним из основных видов горючего для двигателей современной техники.
Автомобильные и мотоциклетные, лодочные и авиационные поршневые двигатели
потребляют бензины. В настоящ ...
Источники поступления
В отраслях
промышленности – основными загрязнителями окружающей среды являются:
электроэнергетика – 0,2%, цветная металлургия – 3%, химические и
нефтепромышленные предприятия – 5%, машиностроение и ...
Алкадиены. Каучук
Алкадиены, или диеновые углеводороды, — непредельные углеводороды,
содержащие в углеродной цепи молекулы две двойные связи.
...


