Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Определение возможного направления протекания реакцииУчим химию / Физическая химия / Учим химию / Физическая химия / Определение возможного направления протекания реакции Определение возможного направления протекания реакции
Для решения этой задачи воспользуемся уравнением Вант-Гоффа:
∆G = (lnПр – lnКр) (17)
где Пр – произведение фактических парциальных давлений газовых компонентов реакции; Кр – константа равновесия реакции при данной температуре.
Напомним, что в соответствии со вторым законом термодинамики и в изобарно – изотермических условиях возможно самопроизвольное протекание процессов, сопровождающихся уменьшением энергии Гиббса системы:
∆G < 0 (18)
В применении к химической реакции это означает, что процесс самопроизвольно может идти слева направо при ∆G < 0 и справа налево при ∆G>0.
Из уравнения (18) следует, что первое условие (∆G < 0) выполняется при Пр<Кр, а второе (∆G>0) – при Пр>Кр.
Таким образом, для ответа на поставленный вопрос необходимо рассчитать константу равновесия при заданной температуре (Т = 1300 К) и величину Пр при содержании H2S – 10 % об., CO2 – 30%, H2O – 30% и COS – 30%, а также общем давлении, равном 1013 гПа. Применяя уравнение (14) найдем величину Кр при 1300 К:
lnKp1300 = (-3765,76 / Т) + 0,33 = (-3765,76 / 1300) + 0,33 = -2,56
Кр1300 = 0,077
В соответствие с уравнением реакции, произведение фактических парциальных давлений запишется в виде
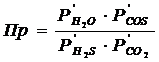 (19)
(19)
где Р/H2S, Р/CO2, Р/H2O, Р/COS – фактические парциальные давления, выраженные в относительных единицах. Для нахождения относительного давления следует давление, выраженное в Паскалях разделить на стандартное давление, равное 101325 Па. Общее давление, выраженное в относительных единицах:
![]()
По закону Дальтона, парциальное давление компонента газовой смеси равно общему давлению, умноженному на объемную долю данного компонента:
Р/H2S = Р/общ ∙0,1 = 0,1
Р/CO2 = Р/общ ∙0,3 = 0,3
Р/H2O = Р/общ ∙0,3 = 0,3
Р/COS = Р/общ ∙0,3 = 0,3
Отсюда произведение парциальных давлений согласно уравнению (19):
![]()
Так как Пр > Кр (3>-2,56), то при заданных условиях ∆G>0 и возможное направление реакции – справа налево, то есть будет происходить диссоциация продукта и будут увеличиваться содержания исходных веществ до тех пор, пока отношение парциальных давлений вновь станет равным Кр.
Смотрите также
Зелинский Николай Дмитриевич
Есть личности, которые олицетворяют собой динамику развития общества и
определяют поступательное движение общественной жизни на многие годы. Право
стать личностью приобретается умением, буду ...
Технология переработки из расплавов аморфных и кристаллизующихся веществ
Промышленность пластмасс развивается сегодня
исключительно высокими темпами. Начиная с 60-х годов, производство полимеров,
основную долю которых составляют пластмассы, удваивается через кажд ...
Общие указания по выполнению
лабораторных работ.
Подготовка к
выполнению лабораторной работы заключается в изучении теоретической части
работы по рекомендованной литературе и по конспектам лекций. В описании
каждой лабораторной работы даны в ...


