Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Разработка способов биосинтетического получения дейтерий-меченhoi
о бактериородопсина. Получение дейтерии-меченного бактериородопсина.Библиотека / Разработка методов биотехнологического получения белков, аминокислот и нуклеозидов, меченных стабильными изотопами 2Н и 13С с высокими степенями изотопного обогащения / Библиотека / Разработка методов биотехнологического получения белков, аминокислот и нуклеозидов, меченных стабильными изотопами 2Н и 13С с высокими степенями изотопного обогащения / Разработка способов биосинтетического получения дейтерий-меченhoi
о бактериородопсина. Получение дейтерии-меченного бактериородопсина. Разработка способов биосинтетического получения дейтерий-меченhoi
о бактериородопсина. Получение дейтерии-меченного бактериородопсина.
В качестве другой модельной системы для введения стабильной изотопной метки в белки, использовали бактериородопсин (bR), синтезируемый в клеточной мембране H. halobium ET 1QOL (рис.6). Для включения дейтериевой метки в bR использовали два принципиально отличных подхода: сайт-специфическое введение отдельных аминокислот: L-[2,3,4,5,6-D5]-Phe, L-[3,5-D2]-Tyr и L-[2,4,5,6,7-D5]-Trp в bR и униформное мечение бактериородопсина дейтерием путем выращивания П. halobium ET 1001 на среде, содержащей 99,9 ат.% тяжёлую воду и дейтеро-гидролизаты В. methylicum.
Бактериородопсин выделяли из пурпурных мембран Н. halobium ET 1001 солюбилизацией в 0,5 %-ном растворе додецилсульфата натрия (ДСН) с последующим осаждением белка метанолом. Гомогенность очищенного bR была потверждена электрофорезом в 12,5%-ном полиакриламидном геле в присутствии 0,1% ДСН (рис.3).
ОФ ВЭЖХ метиловых эфиров Dns-, и Z-производных аминокислот, полученных после гидролиза bR в 4 н. Ва(ОН)2 или 6 н. DCI (3 масс.% фенола, в тяжёлой воде) показала высокие степени хроматографической чистоты выделенных аминокислот и отсутствие примесей небелковой природы в гидролизатах bR. Согласно данным по разделению дериватизованных гидролизатов bR методом ОФ ВЭЖХ, степени хроматографической чистоты выделенных дейтерий-меченных Dns-Phe-OMe, Dns-Tyr-OMe и Dns-Trp-OMe составили 96, 97 и 98% соответственно.
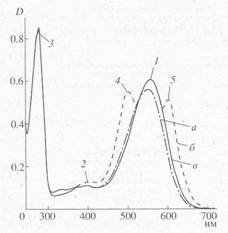
Рис.3. Спектры поглощения бактериородопсина в составе пурпурных мембран H. Halobium в этаноле на различных стадиях обработки: нативный БР (а); пурпурные мембраны после промежуточной обработки (б); очищенный от посторонних каротиноидов БР. Полоса 1 соответствует спектральной форме БР568 ; (2)-примесь спектральной формы М412 ; (3)-посторонние ароматические аминокислоты; (4) и (5)-посторонние каротиноиды. В качестве контроля использован нативный БР
Исследование степени дейтерироваиности бактериородопсина
. Оба подхода показали хорошие результаты по введению дейтериевой метки в молекулу bR. Например, в масс-спектре гидролизата электрофоретически чистого bR, полученного с селективной среды, содержащей L-[2,3,4,5,6-D5]-Phe, L-[3,5-D2]-Tyr и L-2,4,5,6,7-D5]-Trp, после прямой обработки реакционной смеси Dns-Cl и CN2Н2 фиксируются пики, соответствующие молекулярным ионам обогащённых дейтерием Dns-Phe-OMe с М+. при m/z 417 (вместо m/z 412 в контроле), Dns-Tyr-OMe с М+. при m/z 429 (вместо m/z 428) и Dns-Trp-OMe с М+. при m/z 456 {вместо m/z 451).
В случае с униформным мечением bR, метка включалась равномерно по всем положениям углеродного скелета в аминокислотных остатках белка.
Смотрите также
Нефть: происхождение, состав, методы и способы переработки
...
Получение гидроксида натрия каустификацией содового раствора
Гидроксид натрия (каустическая сода) используется
во многих отраслях промышленности: химической, металлургической, нефтеперерабатывающей,
мыловаренной, фармацевтической, целлюлозно-бумажной, ...
Основные химические законы
Когда впервые
обнаруживается, что некоторая идея объясняет или коррелирует многие факты, то
такую идею называют гипотезой. Гипотезу можно подвергнуть дальнейшей
проверке и экспериментально ...


