Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ЦиклобутанОрганическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / Циклобутан ЦиклобутанСтраница 1
По аналогии с циклопропаном циклобутановые скелетные орбитали можно построить из четырех метиленовых единиц:
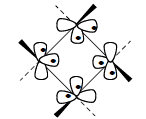
Условимся, что молекула циклобутана имеет плоскую квадратную, а не складчатую, структуру. Используя представления о nσ и nπ-орбиталях, можно построить молекулярные орбитали, показанные на рис. 2.30. Циклобутан имеет пару вырожденный ВЗМО (χ3 и χ4) и пару вырожденных НСМО (χ5 и χ6). Орбитали χ3 и χ4 слабосвязывающие, а орбитали χ5 и χ6 - слаборазрыхляющие, поскольку в них взаимодействуют базисные орбитали атомов углерода, расположенных в противоположных углах четырехчленного цикла ("длинные связи"). Именно по этой причине в циклобутане нарушается правило последовательности орбиталей (σ-π-π*-σ*) и указанные четыре орбитали располагаются между орбиталями χ2 и χ7 вблизи несвязывающего уровня.
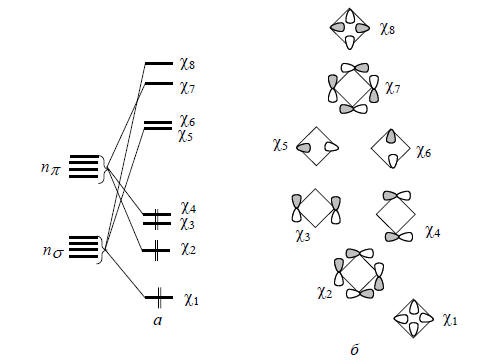 Рис. 2.30. Расщепление nσ- и nπ-орбиталей при образовании циклобутана из четырех метиленовых единиц (а) и форма орбиталей (б)
Рис. 2.30. Расщепление nσ- и nπ-орбиталей при образовании циклобутана из четырех метиленовых единиц (а) и форма орбиталей (б)
Некоторым орбиталям, изображенным на рис. 2.30, можно придать и иную, альтернативную форму. Так, пары орбиталей χ3/χ6 и χ4/χ5 имеют одинаковую симметрию и поэтому могут смешиваться:
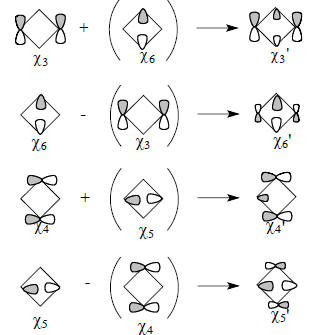
Затем, смешивая пары вырожденных орбиталей χ3'/χ4' и χ5'/χ6' , можно получить альтернативные формы χ3", χ4", χ5" и χ6", которые представляют собой связывающие и антисвязывающие комбинации σ и σ*-орбиталей параллельных связей циклобутанового кольца:
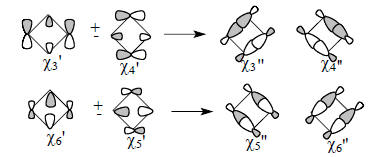
Приведем пример, показывающий, как изображенные на рис. 2.30 молекулярные орбитали можно использовать для объяснения химических свойств молекул, содержащих четырехчленный цикл. Трициклооктадиен (А) легко перегруппировывается в семибульвален через промежуточный бирадикал уже при комнатной температуре. Однако очень похожая молекула трициклического тетраена (Б) абсолютно стабильна.
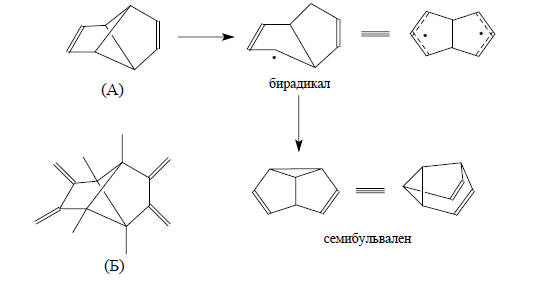
Чтобы объяснить такое различие, сначала заметим, что соединение А представляет собой циклобутановое кольцо с двумя 1,3-этиленовыми мостиками, а соединение Б - циклобутановое кольцо с двумя бутадиеновыми мостиками. Указанное различие между двумя системами можно исследовать на более простых одномостиковых структурах В и Г, к которым мы и перейдем:
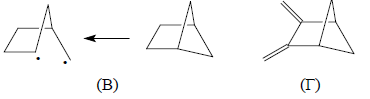
Взаимодействие граничных орбиталей этиленового и циклобутанового фрагментов в соединении В показано на рис. 2.31.
![Рис. 2.31. Орбитальное взаимодействие в 2,3-бис-метиленбицикло[2.2.1]гексане](images/books/251/rozdil151.jpg) Рис. 2.31. Орбитальное взаимодействие в 2,3-бис-метиленбицикло[2.2.1]гексане и форма граничных орбиталей
Рис. 2.31. Орбитальное взаимодействие в 2,3-бис-метиленбицикло[2.2.1]гексане и форма граничных орбиталей
Можно видеть, что вследствие взаимодействия с циклобутановым кольцом энергетическая щель между ВЗМО и НСМО становится меньше, чем в самом этилене. π-Орбиталь перекрывается с заполненной орбиталью χ3 (или χ4) циклобутана, и, таким образом, дестабилизируется, тогда как уровень π*, наоборот, стабилизируется взаимодействием с пустым уровнем χ7.Совершенно противоположный эффект наблюдается в соединении Г с бутадиеновым фрагментом. Энергетическая щель между ВЗМО и НСМО расширяется (если сравнивать с бутадиеном). В данном случае бутадиеновая ВЗМО π2 подходит по симметрии к χ7-орбитали циклобутана и, следовательно, стабилизируется, а НСМО бутадиена π3* дестабилизируется (рис. 2.32). Противоположные результаты, полученные при рассмотрении двух молекул, являются прямым следствием различия в узловых свойствах граничных π-орбиталей этилена и бутадиена (см. рис. 2.8). Молекула В с узкой энергетической щелью между ВЗМО и НСМО должна претерпевать геометрические искажения, которые позволяют орбиталям смешиваться друг с другом (эффект Яна-Теллера второго порядка). Как показано на рис. 2.31, в НСМО бициклического соединения (ψ3) между атомами углерода циклобутанового кольца имеется антисвязывание. Следовательно, при любом асимметрическом искажении молекулы В, позволяющем смешиваться ВЗМО и НСМО, связь между атомами углерода в циклобутановом фрагменте будет ослабляться, что согласуется с легким разрывом связи в этом соединении, приводящим к бирадикалу. В соединении Г щель между ВЗМО и НСМО очень широкая, и вследствие этого исчезает движущая сила для аналогичного эффекта Яна-Теллера. Несмотря на то, что по энергии напряжения цикла соединения В и Г близки, последнее термически гораздо более стабильно.
Смотрите также
Метод суспензионной полимеризации винилхлорида
Термопластичный
полимер поливинилхлорид (ПВХ) – твердое вещество белого цвета, являющееся
продуктом полимеризации винилхлорида, выпускается в виде сыпучего порошка,
готового для дальнейшей ...
Свойства азота
Азот – элемент с седьмым
порядковым номером, относящийся к V главной подгруппе второго периода системы.
По распространенности в земной коре азот занимаем 31-е место – 0,025% (по
другим данн ...
Ядерная химия
Наряду со стабильными изотопами
данного химического элемента известны многочисленные изотопы химических
элементов, способные самопроизвольно превращаться в изотопы других химических
элементов посре ...


