Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Плоскостные σ-орбитали малых циклов. ЦиклопропанОрганическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / Плоскостные σ-орбитали малых циклов. Циклопропан Плоскостные σ-орбитали малых циклов. ЦиклопропанСтраница 1
Молекулу циклопропана можно рассматривать как состоящую из трех метиленовых единиц ("строительных блоков"), каждая из которых имеет орбитали, используемые для образования связей С-Н (на схеме не показаны), и, кроме того, nσ- и nπ-орбитали, используемые для образования скелетных связей С-С:
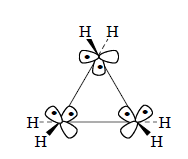
nπ-Орбитали по энергии расположены немного выше nσ -орбиталей. Форма скелетных плоскостных орбиталей и последовательные стадии их построения, включающие первоначальное объединение двух атомов и последующее присоединение третьего атома углерода, показаны на рис. 2.29. Расщепление уровней (рис. 2.29,а) соответствует общему правилу, согласно которому самую низкую энергию имеют σ-орбитали, а самую высокую энергию - орбитали σ*-типа; между ними располагаются π- и π*-орбитали.
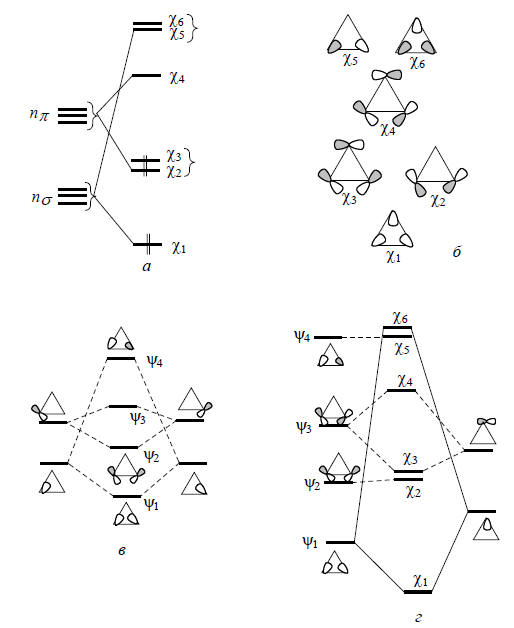 Рис. 2.29. Расщепление nσ- и nπ-орбиталей при образовании скелетных плоскостных орбиталей циклопропана (а); форма орбиталей (б) и последовательные стадии построения орбиталей цикла (в и г).
Рис. 2.29. Расщепление nσ- и nπ-орбиталей при образовании скелетных плоскостных орбиталей циклопропана (а); форма орбиталей (б) и последовательные стадии построения орбиталей цикла (в и г).
Более строгая форма скелетных циклопропановых орбиталей получается при учете того факта, что орбитали χ5 и χ6 имеют ту же симметрию, что и орбитали χ2 и χ3. Следовательно, они смешиваются друг с другом, что показано ниже:
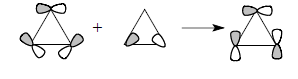
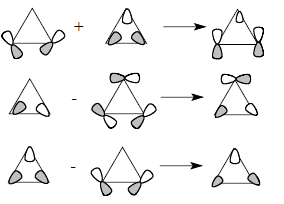
Орбитали циклопропана не имеют четко выраженного направления вдоль межъядерной линии С-С, и связи С-С поэтому называются "банановыми" (гл. 24). Плоскостные σ-орбитали (рис. 2.29,б) соответствуют трем С-С-связям цикла, и каждая из связывающих орбиталей χ1, χ2 и χ3 занята парой электронов. Орбитали χ2 и χ3 лежат выше, чем обычные σсс-орбитали, например, в этане. Они почти целиком построены из р-орбиталей атома углерода, лежащих в плоскости цикла. Эти р-орбитали в отличие от циклоалканов с большими размерами цикла направлены друг к другу не по линии С-С-связей. Следовательно, вырожденные уровни χ2 и χ3, в принципе, должны быть хорошими электронодонорами по отношению к заместителям в трехчленном цикле. По той же причине орбиталь χ4 (НСМО) должна обладать хорошими акцепторными свойствами. Три С-С-связи в циклопропане эквивалентны, поскольку орбитали в паре χ2/χ3 заняты. Однако орбиталь χ2 и χ3 по-разному взаимодействуют с заместителями в кольце. Например, диметил-циклопропильный карбокатион более стабилен в конформации (А), чем в кон-формации (Б), причем барьер вращения между этими двумя формами очень вы-сок (∼14 ккал/моль по данным ЯМР).Этот факт очень легко объяснить взаимо-действием карбокатионной р-орбитали с циклопропановой орбиталью χ3:
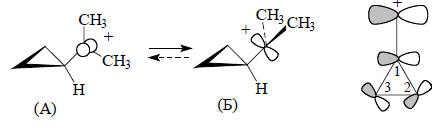
Результатом такого взаимодействия является ослабление связей С(1)-С(2) и С(1)-С(3) и усиление связи С(2)-С(3) в производных циклопропана, содержащих хорошие электроноакцепторные заместители (CR2, -C≡N, -COOR), что выражается в удлинении связей С(1)-С(2) и С(1)-С(3) и укорочении связи С(2)-С(3). Типичный пример приведен ниже:
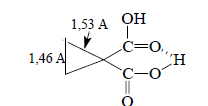
Аналогично, можно легко понять, почему положение равновесия норкарадиен - гептатриен сдвинуто в сторону норкарадиена при наличии сильных электроноакцепторных заместителей R:
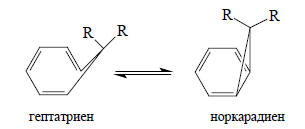
Циклопропильный фрагмент норкарадиена стабилизируется электроноакцепторными группами. Если R=H, то соединение существует только в циклогептатриеновой форме, но если R=CN, равновесие сдвинуто в сторону норкарадиена.Орбиталь χ2 (вторая вырожденная ВЗМО) отвечает за протонирование циклопропана "по ребру":
Смотрите также
Компоненты, обладающие свойствами понижать горючесть полимерных материалов
Ежегодно пожары
наносят экономике страны ущерб в сотни миллионов рублей. При сгорании
полимерных материалов выделяется большое количество токсичных газов, пагубно
действующих на человека и ...
Общие свойства молекулярных орбиталей
Общие
свойства МО хюккелевских УВ:
Альтернантность.
Теорема парности.
Свойства
корней векового детерминанта.
Матрица
коэффициентов (составы МО).
Свойства
коэффициентов.
П ...
Технология нуклеофильного замещения функциональных групп в органических соединениях
Атом
галогена в молекуле органического соединения с успехом может быть замещен на
другие группы атомов, что создает широкие возможности для синтеза биологически
активных соединений, исходя ...


