Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Орбитали фрагментов молекул и их использованиеОрганическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / Орбитали фрагментов молекул и их использование Орбитали фрагментов молекул и их использованиеСтраница 2
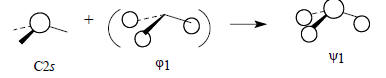
Вследствие этого орбиталь ψ1 имеет характер орбиталей s, ϕ1 и pz. Если, как мы делали раньше, пренебречь влиянием малого возмущения со стороны pz-орбитали, то у орбитали ψ1 останется лишь характер s и ϕ1 -орбиталей:
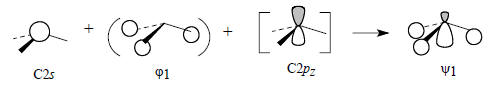
Орбиталь ψ5 образуется следующим образом:
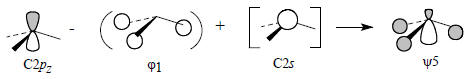
Пренебрегая членом в квадратных скобках, получим более простую картину:
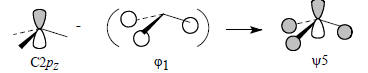
В дальнейшем мы часто будем использовать самые простые эскизы орбиталей типа ψ1 и ψ5, пренебрегая слабым возмущением со стороны орбиталей, взятых в квадратные скобки.При образовании орбитали ψ5 взаимодействие с групповой орбиталью ϕ1 Н3 происходит в противофазе. Поэтому орбиталь можно рассматривать как типичную антисвязывающую орбиталь с высокой энергией.Вырожденные пары связывающих (ψ2 и ψ3) и разрыхляющих (ψ6 и ψ7) орбиталей образуются путем парных взаимодействий между орбиталями Н3 и С, имеющими подходящую друг другу симметрию. Связывающая и несвязывающая комбинации рх и ϕ2 дают соответственно ψ2 и ψ6, а при комбинации ру и ϕ3 образуются ψ3 и ψ7.
Смотрите также
Обсуждение полученных результатов.
Исходя из результатов синтеза, можно сделать вывод о том, что:
- серная кислота является хорошим катализатором для данной реакции;
-поддерживаемая температура оказалась благоприятной для про ...
Приготовление основных стандартных растворов металлов с
концентрацией
1.
Средства измерений, реактивы, оборудование
Весы
лабораторные аналитические любого типа 2-го класса точности
Колбы
мерные наливные : 2-1000-2 по ГОСТ 1770
Цилиндры
мерные: 1-50 по ГОСТ ...
Пластические массы
Термин
"пластические массы" появился в конце XIX в. Первые промышленные материалы
были изготовлены на основе нитроцеллюлозы (1862-65) и казеина (1897). Развитие
современных реакто ...


