Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Современные представления о
химической связиОткрытая химия / Химическая связь / Открытая химия / Химическая связь / Современные представления о
химической связи Современные представления о
химической связи
Совокупность химически связанных атомов (молекула, кристалл) состоит из атомных ядер и связанных с ними электронов. Положение атомных ядер экспериментально устанавливается довольно точно. Распределение электронной плотности фиксируется менее точно, поскольку в молекуле каждый из валентных электронов может быть обнаружен в окрестности любого ядра. Тем не менее каждому из этих валентных электронов, как и в атоме, соответствует определенный энергетический уровень, называемый молекулярной орбиталью (МО). При построении молекулярных орбиталей используется метод линейной комбинации атомных орбиталей (ЛКАО), обозначаемый аббревиатурой МО – ЛКАО.
Кроме этого подхода рассмотрим метод валентных связей (МВС), основанный на предположении, что химическая связь осуществляется одной или несколькими электронными парами, локализованными между взаимодействующими атомами.
|
|
|
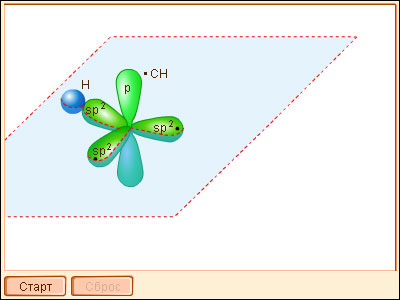
Модель 3.2. Связи в молекуле бензола |
Смотрите также
Химические реакции. Реакции в растворах электролитов
...
Химические свойства неметаллов и их соединений
...
Электролиз.
Цель работы - ознакомление
с процессами, протекающими на растворимых и нерастворимых электродах при
электролизе водных растворов электролитов.
Электролиз - это
окислительно-восстановительный ...