Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Структура и формы льда.Библиотека / Необычные свойства обычной воды / Библиотека / Необычные свойства обычной воды / Структура и формы льда. Структура и формы льда.Страница 1
Вода при охлаждении в нормальных условиях ниже 0о С кристаллизируется, образуя лед, плотность которого меньше, а объем почти на 10% больше объема исходной воды. Охлаждаясь, вода ведет себя как многие другие соединения: понемногу уплотняется-уменьшает свой удельный объем. Но при 4 оС ( точнее, при 3,98 оС) наступает кризисное состояние: при дальнейшем понижении температуры объем воды уже не уменьшается, а увеличивается. С этого момента начинается упорядочение взаимного расположения молекул, складывается характерная для льда гексагональная кристаллическая структура. Каждая молекула в структуре льда соединена водородными связями с четырьмя другими. Это приводит к тому, что в фазе льда образуется ажурная конструкция с " каналами" между фиксированными молекулами воды. В водных растворах некоторых органических веществ вокруг молекул примесей возникают упорядоченные группы водных молекул своеобразные зоны "жидкого льда", имеющие кубическую структуру, которая отличается большой рыхлостью по сравнению с гексагональной. Появление такого льда вызывает значительное расширение всей замерзшей массы. При появлении льда разрушаются связи не только дальнего, но и ближнего порядка. Так, при 0 о С 9- 15% молекул Н2О утрачивают связи с соединениями, в результате увеличивается подвижность части молекул и они погружаются в те полости, которыми богата ажурная структура льда. Этим объясняется сжатие льда при таянии и большая по сравнению с ним плотность образующейся воды. При переходе " лед-вода" плотность возрастает примерно на 10%, и можно считать, что эта величина определенным образом характеризует количество молекул Н2О, попавших в полости.
В твердой воде (лед) атом кислорода каждой молекулы участвует в образовании двух водородных связей с соседними молекулами воды согласно схеме, в которой водородные связи показаны пунктиром
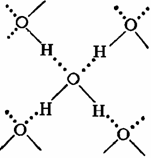
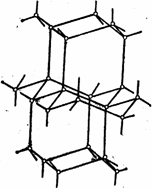
Образование водородных связей приводит к такому расположению молекул воды, при котором они соприкасаются друг с другом своими разноименными полюсами. Молекулы образуют слои, причем каждая из них связана с тремя молекулами, принадлежащими к тому же слою, и с одной — из соседнего слоя. Структура льда принадлежит к наименее плотным структурам, в ней существуют пустоты, размеры наименее плотным структурам, в ней существуют пустоты, размеры которых несколько превышают размеры молекулы ![]() .
.
Характерной особенностью структуры льда является то, что в ней молекулы упакованы рыхло. Если изобразить молекулу шаром, то при плотневшей упаковке шаров вокруг каждого из них будет 12 соседей . Во льду же их всего четыре. Если бы молекулы воды во льду были плотно упакованы, то его плотность составляла бы 2,0 г/см3, тогда как на самом деле она равна 0,92 г/см3. Казалось бы, рыхлость упаковки частиц, то есть наличие в ней больших объемов не заполненного молекулами пространства, должна приводить к неустойчивости структуры. Например, можно было бы ожидать, что при сжатии льда внешним давлением сетка водородных связей будет разрушаться, пустоты структуры будут с легкостью схлопываться, заполняясь молекулами, вырванными из этой сетки. Но не тут-то было! На самом деле сетка водородных связей не разрушается, а перестраивается. При повышении давления обычный гексагональный лед меняет свою структуру.
Сейчас известно десять форм льда, устойчивых при высоких давлениях. И у всех сохраняется четырежды координированная сетка водородных связей, то есть каждая молекула воды сохраняет в них все свои четыре водородные связи.
I – обычный лед, существующий при давлении до 2200 атм., при дальнейшем увеличении давления переходит в II;
II – лед с уменьшением объема на 18%, тонет в воде, очень неустойчив и легко переходит в III;
III – также тяжелее воды и может непосредственно быть получен из льда I;
IV – легче воды, существует при небольших давлениях и температуре немного ниже 0° С, неустойчив и легко переходит в лед I;
V – может существовать при давлениях от 3600 до 6300 атм., он плотнее льда III, при повышении давления с треском мгновенно превращается в лед VI;
VI – плотнее льда V, при давлении около 21 000 атм. имеет температуру +76° С; может быть получен непосредственно воды при температуре +60° С и давлении 16 500 атм.
Структура льда , у которой все углы между соседними водородными связями равны тетраэдрическому углу , обладает минимальной плотностью (наибольшей рыхлостью), возможной для четырежды координированных сеток. При деформации такой сетки плотность
неизбежно увеличивается, так что, например, для льда III она составляет 1,15 г/см3, то есть на 25% больше, чем во льду .
Смотрите также
Расчёт многокорпусной выпарной установки
В химической промышленности выпариванию подвергают
растворы твердых веществ (главным образом водные растворы щелочей, солей и
др.), а также растворы высококипящих жидкостей, обладающих при т ...
Атомы и молекулы
Любое вещество состоит из ничтожно малых частиц – так называемых атомов. Часто атомы объединяются в группы, которые называют молекулами. Размеры атомов настолько малы, что увидеть их через обычн ...
Изучение и анализ производства медного купороса
Целью
данного дипломного проекта является изучение и анализ производства медного
купороса, основанного на переработке отработанного передаточного электролита
цеха электролиза меди.
В
хо ...


