Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Масса вещества (объем газа) по известному количеству другого
реагента (продукта)Cправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Cправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Масса вещества (объем газа) по известному количеству другого
реагента (продукта) Масса вещества (объем газа) по известному количеству другого
реагента (продукта)Страница 1
Примеры решения задачи
1. Прокалили 66,6 г минерала малахит Cu2СO3(OН)2. Установите объем (в литрах, н.у.) собранного газа.
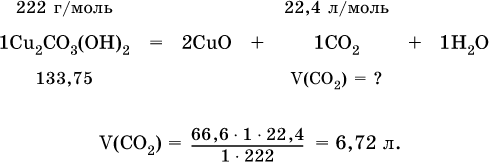
2. Определите суммарный объем (в литрах, н.у.) газов, полученных при термическом разложении 133,75 г хлорида аммония.
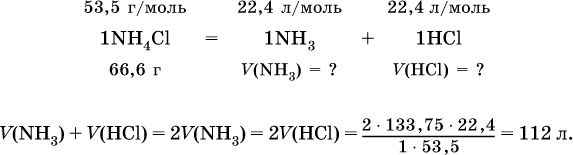
Задания для самостоятельного решения части В
1. Какой объем (в литрах, н.у.) газа выделяется при обработке водой смеси 0,2 моль натрия и 1,4 г лития?
2. При действии избытка воды на 10 г некоторого металла из главной подгруппы II группы выделилось 5,6 (н.у.) газа. О каком металле идет речь?
3. В концентрированный раствор щелочи вносят 2,7 г алюминия. Найдите объем (в литрах, н.у.) собранного газа.
4. На сжигание 0,64 г металла расходуется 12 мл (н.у.) кислорода. Какой металл был взят?
5. Металлическая пластинка массой 50 г после пребывания в соляной кислоте уменьшилась на 1,68 % (по массе), при этом выделилось 0,336 л (н.у.) газа. Из какого металла изготовлена пластинка?
6. При нагревании 139,2 г оксида металла (I) выделилось 6,72 л (н.у.) газа. Оксид какого металла был использован?
7. После обработки равномолярной смеси Mg + Zn избытком едкого натра (конц.) образовалось 4,48 л (н.у.) газа. Рассчитайте массу (в граммах) исходной смеси.
8. Установите объем (в литрах, н.у.) хлора, вступившего в реакцию со щелочью в горячем растворе, если образовалось 0,46 моль хлорид‑ионов.
9. Вычислите объем (в литрах, н.у.) полученного газа, если в реакцию с кипящей серной кислотой (конц.) вступило O,5 моль фторида кальция.
10. Сероводород (4,48 л при н.у.) смешали с избытком диоксида серы. Какова масса (в граммах) твердого продукта этой реакции?
11. Поглощение 5,6 л (н.у.) сероводорода раствором нитрата висмута (III) приводит к выпадению осадка средней соли. Найдите массу (в граммах) этого осадка.
12. Раствор гидроксида цезия поглотил 17,92 л (н.у.) диоксида серы с образованием средней соли. Вычислите массу (в граммах) щелочи, истраченной на реакцию.
13. Прокалили 99,3 г нитрата свинца (II). Определите суммарный объем (в литрах, н.у.) полученных газов.
14. В избыток воды внесено 3,75 моль оксида фосфора (V). Какая масса (в граммах) продукта образовалась?
15. Прокаливанием 192 г карбоната аммония получена смесь двух газов и вода. Установите общий объем (в литрах, н.у.) смеси.
16. Внесено 14 г аморфного кремния в концентрированный раствор едкого натра. Рассчитайте объем (в литрах, н.у.) собранного газа.
17. Какой объем в литрах (н.у.) хлора потребуется для получения из метана 4 моль хлороформа?
18. Найдите количество бромэтана (моль), вступившее в реакцию с натрием, если образовалось 237 л (н.у.) органического продукта.
19. Ацетилен обесцвечивает бромную воду с образованием 3,46 г конечного продукта. Определите объем (мл, н.у.) затраченного алкина.
20. Каталитическая реакция дегидрирования 49 г метилциклогексана приводит к получению гомолога бензола. Вычислите объем (в литрах, н.у.) образовавшегося одновременно газа.
21. Этанол с плотностью 0,8 г/мл затрачен на получение 44,8 л (н.у.) дивинила. Установите расход (мл) спирта.
Смотрите также
Осаждение частиц
...
Реакции фенолов
Фенолы могут реагировать как
по гидроксильной группе, так и по бензольному кольцу.
...


