Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Нитриты. НитратыCправочник по химии для подготовки к ЕГЭ / Неметаллы главных подгрупп IV–VII групп / Cправочник по химии для подготовки к ЕГЭ / Неметаллы главных подгрупп IV–VII групп / Нитриты. Нитраты Нитриты. Нитраты
Нитрит калия
KNO2. Оксосоль. Белый, гигроскопичный. Плавится без разложения. Устойчив в сухом воздухе. Очень хорошо растворим в воде (образуется бесцветный раствор), гидролизуется по аниону. Типичный окислитель и восстановитель в кислотной среде, очень медленно реагирует в щелочной среде. Вступает в реакции ионного обмена. Качественные реакции на ион NO2‑ – обесцвечивание фиолетового раствора MnO4 и появление черного осадка при добавлении ионов I‑. Применяется в производстве красителей, как аналитический реагент на аминокислоты и иодиды, компонент фотографических реактивов.
Уравнения важнейших реакций:
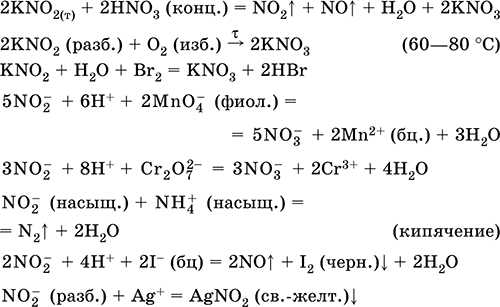
Получение в промышленности– восстановлением калийной селитры в процессах:
KNO3 + Pb = KNO2+ PbO (350–400 °C)
KNO3 (конц.) + Pb (губка) + Н2O = KNO2+ Pb(OH)2↓
2KNO3 + СаО + SO2 = 2KNO2
+ CaSO4 (300 °C)
Нитрат калия KNO3.
Оксосоль. Техническое название калийная, или индийская, селитра. Белый, плавится без разложения, при дальнейшем нагревании разлагается. Устойчив на воздухе. Хорошо растворим в воде (с высоким эндо‑эффектом, Q = ‑36 кДж), гидролиза нет. Сильный окислитель при сплавлении (за счет выделения атомарного кислорода). В растворе восстанавливается только атомарным водородом (в кислотной среде до KNO2, в щелочной среде до NH3).
Применяется в производстве стекла, как консервант пищевых продуктов, компонент пиротехнических смесей и минеральных удобрений.
Уравнения важнейших реакций:
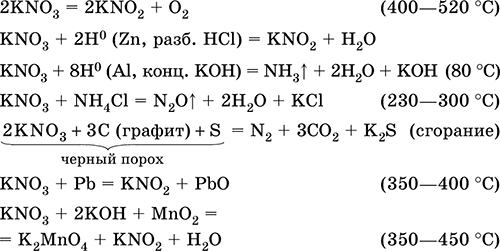
Получение: в промышленности
4KOH (гор.) + 4NO2 + O2 = 4KNO3
+ 2Н2O
и в лаборатории
:
КCl + AgNO3 = KNO3+ AgCl↓
Смотрите также
Осмий - благородный металл
ОСМИЙ
(лат. Osmium), Os, химический элемент VIII группы периодической системы,
атомный номер 76, атомная масса 190,2, относится к платиновым металлам.
...
Свойство водных растворов
электролитов.
Цель
работы:
ознакомится с электропроводностью растворов, ионными равновесиями в растворах
электролитов.
Согласно
теории электролитической диссоциации электролиты при растворении в воде
распад ...
Монослой на
основе фуллеренов и краун-эфиров
Проведенные
исследования [3-5] показали, что молекулы С60 при степени покрытия 0,4-0,5
начинают агрегировать уже в газовой фазе, что исключает возможность
формирования монослоя и, как следствие, во ...


