Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Кинетические изотопные эффектыСтатьи и работы по химии / Дискриминация гипотез по кинетическим экспериментам / Статьи и работы по химии / Дискриминация гипотез по кинетическим экспериментам / Кинетические изотопные эффекты Кинетические изотопные эффектыСтраница 1
Первичным кинетическим изотопным эффектом называют различие в скоростях разрыва (образования) химических связей при замене одного из атомов рвущейся (образующейся) связи его изотопом.
В основе первичного КИЭ при разрыве или образовании связи, например, С-Н, лежит различие величин нулевой энергии колебательного уровня этой связи, зависящей от природы изотопов, например, С (12С, 13С, 14С) или Н (1Н, 2D, 3T). Так, нулевая энергия связи U0 C-H ~ на 5 кДж/моль выше U0 для С-D. Поскольку соответствующие частоты колебаний в переходном состоянии в значительно меньшей степени зависят от массы изотопа (при наличии других тяжелых атомов и групп в реагентах), энергия активации в случае более легкого изотопа (С-Н) будет также ниже энергии активации для С-D и С-Т. Максимальные КИЭ разрыва связи без учета образования новых связей составляют: Срочный выкуп авто.
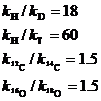
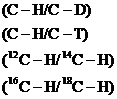
Поскольку в переходном состоянии связь рвется не полностью, максимальные значения КИЭ не достигаются. Величина КИЭ будет тем больше, чем в большей степени связи C-X, M-X, M-H разрываются в переходном состоянии.
Из теоретического анализа простой реакции переноса протона
![]()
в апротонных растворителях сделаны следующие выводы:
1) Основной вклад в КИЭ по водороду вносит потеря энергии валентного колебания связи А–Н при образовании переходного состояния. Частоты валентных колебаний в переходном состоянии ниже, чем в начальном и в меньшей степени зависят от массы изотопа.
2) Величина КИЭ определяется главным образом разностью энергий активации, а не отношением предэкспонентов.
3) Значения КИЭ обычно меньше, чем это следует из значений нулевых частот колебаний связей А–Н и A–D.
4) При использовании трех изотопов 1H, 2D и 3Т выполняется соотношение
![]()
Если связь в реагенте рвется в лимитирующей стадии, можно ожидать при замене, например H на D, значительного КИЭ. Так, в реакции
![]()
КИЭ ![]() . Это означает, что именно связь C-D рвется в лимитирующей стадии. В квазиравновесных стадиях наблюдаются равновесные (термодинамические) изотопные эффекты (ТИЭ).
. Это означает, что именно связь C-D рвется в лимитирующей стадии. В квазиравновесных стадиях наблюдаются равновесные (термодинамические) изотопные эффекты (ТИЭ).
Пример. При исследовании реакции окисления этилена хлоридом Pd(II) (Вакер-процесс) было обнаружено, что в реакциях
![]()
![]()
![]() и все четыре атома D переходят в ацетальдегид. Следовательно, С-Н связь не рвется в лимитирующей стадии. Вместе с тем, при замене H на D в воде
и все четыре атома D переходят в ацетальдегид. Следовательно, С-Н связь не рвется в лимитирующей стадии. Вместе с тем, при замене H на D в воде ![]() . Этот эффект, судя по кинетике процесса есть ТИЭ, появление которого связано с разницей констант автопротолиза Kw D2O и H2O (Kw H2O в 5.13 раз выше Kw D2O), и, соответственно, констант кислотной диссоциации аквакомплексов палладия(II).
. Этот эффект, судя по кинетике процесса есть ТИЭ, появление которого связано с разницей констант автопротолиза Kw D2O и H2O (Kw H2O в 5.13 раз выше Kw D2O), и, соответственно, констант кислотной диссоциации аквакомплексов палладия(II).
Пример. При изучении кинетики реакций окислительного карбонилирования ацетилена в растворах комплексов Pd(I) с образованием ангидридов малеиновой (МА) и янтарной (ЯА) кислот, акриловой (АК) и пропионовой (ПК) кислот установлено, что МА и ЯА образуются с КИЭ ~ 1.
Смотрите также
Типы реакций и их классификация в органической химии
...
Круговорот золота в природе
...
Гидролиз солей.
Цель работы -
изучение некоторых реакций обмена между электролитами; изучение водных
растворов солей, связанных с реакцией гидролиза. ...


