Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Влияние ионной силы на скорость реакции.Статьи и работы по химии / Гомогенный катализ / Статьи и работы по химии / Гомогенный катализ / Влияние ионной силы на скорость реакции. Влияние ионной силы на скорость реакции.Страница 1
Во всех уравнениях химической кинетики фигурируют концентрации реагирующих веществ. В термодинамике же константа равновесия неидеальной системы выражается через активности. Это обстоятельство необходимо учитывать, если в кинетическое уравнение входит константа равновесия. Правда, при реакциях в газовой фазе и между нейтральными молекулами в растворе в этом нет практической необходимости, но при рассмотрении реакций между заряженными частицами подобное пренебрежение может явиться источником существенных ошибок. Для константы скорости бимолекулярной реакции
![]()
протекающей в растворе, теория активного комплекса дает
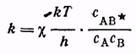
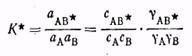 Термодинамическая же константа равновесия между исходными веществами и активным комплексом
Термодинамическая же константа равновесия между исходными веществами и активным комплексом
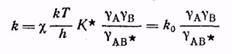 |
Комбинируя эти уравнения получаем уравнение Бренстеда-Бьеррума:
Для константы скорости реакции, протекающей в любой неидеальной среде. Величина k0 имеет смысл константы скорости при бесконечном разведении, т. е. при γ=1.
где А—постоянная, равная для водных растворов при 25° С примерно 0,51
z — заряд иона;
I — ионная сила раствора;
b — некоторая постоянная, примерно обратно пропорциональная радиусу иона.
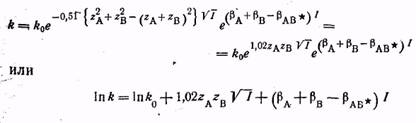 |
Рассмотрим два случая:
1. Взаимодействие между заряженными частицами.
Смотрите также
Никель и его карбонил
Основой
современной техники являются металлы и металлические сплавы. Разнообразные
требования к металлическим материалам возрастают по мере развития новых отраслей
техники.
В наше время ...
Пирит
Пирит - минерал,
дисульфид железа FeS2, самый распространенный в земной коре сульфид.
Другие названия минерала и его разновидностей: кошачье золото, золото дурака,
железный колчедан, марказит, брав ...
Полимераналогичные превращения хитозана
Макромолекула
хитозана является линейной и не содержит ни поперечных связей, ни разветвлений.
Изучению свойств и химических реакций хитозана посвящено много работ. Наиболее
полные данные пр ...


