Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ТестСтатьи и работы по химии / Гомогенное химическое равновесие / Статьи и работы по химии / Гомогенное химическое равновесие / Тест ТестСтраница 1
В вопросах 1-10 необходимо выбрать правильный ответ (он может быть только один).
1. При наступлении состояния химического равновесия протекают следующие процессы:
а) число молекул веществ, составляющих химическую систему увеличивается во времени при неизменных внешних условиях;
б) число молекул веществ, составляющих химическую систему остаётся постоянным во времени при неизменных внешних условиях;
в) число молекул веществ, составляющих химическую систему, уменьшается во времени при неизменных внешних условиях.
2. Для реакции: ![]() протекающей в изобарно-изотермических условиях, общее выражение для изменения энергии Гиббса имеет вид:
протекающей в изобарно-изотермических условиях, общее выражение для изменения энергии Гиббса имеет вид:
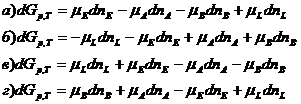
3. Для состояния химического равновесия характерно:
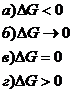
4. Уравнение изотермы химической реакции имеет вид:
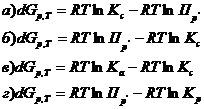
5. Для реакции: ![]()
Константа равновесия, выраженная через парциальные давления газов, записывается так:
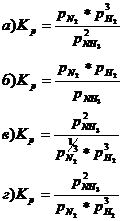
6. Какое из выражений соответствует уравнению изобары химической реакции:
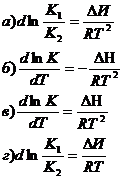
7. Стандартная константа равновесия связана с константой равновесия Кр соотношением:
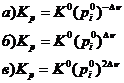
![]()
8. Для реакции в газовой фазе, протекающей без изменения числа молей (Δν=0) характерно:
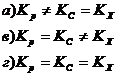
9. Связь между Кр и Кс химической реакции выражается уравнением:
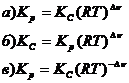
10. В общем виде Кх для реакции: ![]() можно выразить так:
можно выразить так:
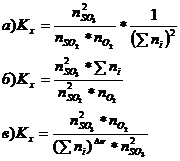
Правильные ответы:
|
№ вопроса |
Ответ |
|
1. |
б) |
|
2. |
в) |
|
3. |
в) |
|
4. |
г) |
|
5. |
г) |
|
6. |
в) |
|
7. |
б) |
|
8. |
в) |
|
9. |
а) |
|
10. |
б) |
Смотрите также
Результаты экспериментов
Таблица 3.4.
Экспериментальные
данные по окислительному карбонилированию фенилацетилена и метилацетилена.
Иссл.
система
Дата
Реагирующая система
...
Зависимость типа и размера мицелл от концентрации ПАВ
...
Процесс компаундирования нефтепродуктов
Промышленное
производство
нефтепродуктов состоит из следующих основных этапов: первичная, вторичная
переработка нефти и процессы смешения (компаундирования).
Первичная
переработка
(пря ...


