Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Квантовые числа электронаОткрытая химия / Электронное строение атомов / Открытая химия / Электронное строение атомов / Квантовые числа электрона Квантовые числа электронаСтраница 1
Квантовое число n – главное. Оно определяет энергию электрона в атоме водорода и одноэлектронных системах (He+, Li2+ и т. д.). В этом случае энергия электрона
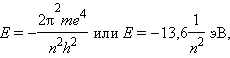 |
где n принимает значения от 1 до ∞. Чем меньше n, тем больше энергия взаимодействия электрона с ядром. При n = 1 атом водорода находится в основном состоянии, при n > 1 – в возбужденном.
В многоэлектронных атомах электроны с одинаковыми значениями n образуют слой или уровень, обозначаемый буквами K, L, M, N, O, P и Q. Буква K соответствует первому уровню, L – второму и т. д.
|
|
|
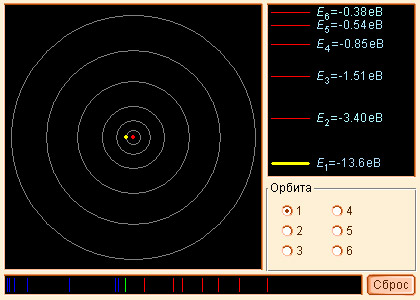
Модель 2.2. Атом водорода |
Орбитальное квантовое число l характеризует форму орбиталей и принимает значения от 0 до n – 1. Кроме числовых l имеет буквенные обозначения
|
l |
= |
0 |
1 |
2 |
3 |
4 |
… |
|
l |
= |
s |
p |
d |
f |
g |
… |
Электроны с одинаковым значением l образуют подуровень.
Квантовое число l определяет квантование орбитального момента количества движения электрона ![]() в сферически симметричном кулоновском поле ядра.
в сферически симметричном кулоновском поле ядра.
Квантовое число ml называют магнитным. Оно определяет пространственное расположение атомной орбитали и принимает целые значения от –l до +l через нуль, то есть 2l + 1 значений. Расположение орбитали характеризуется значением проекции вектора орбитального момента количества движения Mz на какую-либо ось координат (обычно ось z):
| |
Все вышесказанное можно представить таблицей:
| ||||||||||||||||||
|
Таблица 2.1 Число орбиталей на энергетических подуровнях |
Смотрите также
Глюкоза
...
Разработка методов и средств реабилитации объектов отравляющих веществ
Обеспечение безопасности людей и защита окружающей среды (ОС)
являются основополагающими требованиями Конвенции о запрещении разработки,
производства, накопления и применения химического ору ...