Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Коагуляция дисперсной системы. Скорость коагуляции. Причины,
вызывающие процесс самопроизвольной коагуляции.Статьи и работы по химии / Вычисление теплового эффекта реакций / Статьи и работы по химии / Вычисление теплового эффекта реакций / Коагуляция дисперсной системы. Скорость коагуляции. Причины,
вызывающие процесс самопроизвольной коагуляции. Коагуляция дисперсной системы. Скорость коагуляции. Причины,
вызывающие процесс самопроизвольной коагуляции.
Коагуляция – процесс самопроизвольного укрупнения (слипания) дисперсных частиц, который может происходить при действии на дисперсную систему различных факторов: при интенсивном перемешивании или встряхивании, нагреве или охлаждении, облучении светом или пропускании электрического тока, при добавлении к системе электролитов или неэлектролитов и др. При разных способах воздействия на систему происходит уменьшение энергии связи диспергированных частиц с окружающей их дисперсионной средой. Так, добавление электролита вызывает сжатие диффузного слоя в коллоидной частице, следовательно, понижение величины электрокинетического потенциала. Это приводит к уменьшению электростатического отталкивания коллоидных частиц и, как следствие, к большей вероятности их слипания.
Минимальная концентрация электролита, добавляемого к дисперсной системе, при которой наступает явная коагуляция за определенный промежуток времени, носит название порога коагуляции ![]() . Порог коагуляции определяется температурой, природой добавленного электролита, знаком заряда добавляемого иона (действует прежде всего ион, имеющий заряд, противоположный заряду коллоидных частиц) и величиной заряда этого иона. Так, для трех-, двух- и однозарядных ионов явная коагуляция наступает при концентрации электролитов в соотношении 1:10 - 50: 500-1000 (приближенное правило Шульце-Гарди).
. Порог коагуляции определяется температурой, природой добавленного электролита, знаком заряда добавляемого иона (действует прежде всего ион, имеющий заряд, противоположный заряду коллоидных частиц) и величиной заряда этого иона. Так, для трех-, двух- и однозарядных ионов явная коагуляция наступает при концентрации электролитов в соотношении 1:10 - 50: 500-1000 (приближенное правило Шульце-Гарди).
Порог коагуляции рассчитывается следующим образом:
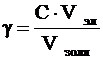 , (1)
, (1)
где g - порог коагуляции, кмоль/м3;
С – молярная концентрация раствора электролита, кмоль/м3;
Vэл – объем раствора электролита, м3;
Vзоля – объем золя, м3.
Теорию быстрой скорости коагуляции разработал Смолуховский. Он автор уравнения для расчета константы скорости коагуляции K:
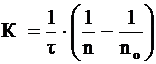 , (2)
, (2)
где n0 и n – число частиц в единице объема системы до начала коагуляции и к моменту времени ![]() соответственно;
соответственно;
t - время коагуляции, с.
Константа скорости коагуляции зависит от коэффициента диффузии для частиц и их радиуса следующим образом:
К = 8 · p · D · r. (3)
Учитывая уравнение (2) и уравнение Эйнштейна, окончательное уравнение для константы скорости коагуляции принимает вид:
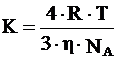 , (4)
, (4)
где К – константа скорости коагуляции, м3/с;
![]() – вязкость среды, Па·с;
– вязкость среды, Па·с;
NA – число Авогадро.
Смолуховский ввел также понятие о времени половинной коагуляции, согласно которому время, необходимое для уменьшения первоначального числа частиц в 2 раза, связано с их исходным числом следующим образом:
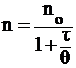 , (5)
, (5)
где q – время половинной коагуляции, с;
t – время от начала коагуляции, с.
Из уравнения, преобразованного к виду:
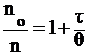 , (6)
, (6)
следует, что если построенный в координатах nо/n = f (t) график представляет собой прямую линию, то это служит показателем соответствия экспериментальных данных теории Смолуховского.
Смотрите также
Методика проведения потенциометрического титрования.
Рассмотрим процесс
потенциометрического титрования сильной кислоты раствором сильной щелочи. ...
Химия актиноидов (актинидов)
...
Олово
...


