Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Билет №12 (углубленно).Статьи и работы по химии / Билеты по химии 10 класс / Статьи и работы по химии / Билеты по химии 10 класс / Билет №12 (углубленно). Билет №12 (углубленно).Страница 2
Для получения высокоактивных металлов (натрия, алюминия, магния, кальция и др.), легко вступающих во взаимодействие с водой, применяют электролиз расплава солей:
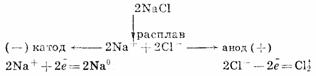
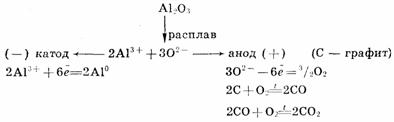
Зависимость количества вещества, образовавшегося под действием электрического тока, от времени, силы тока и природы электролита может быть установлена на основании обобщенного закона Фа-радея:
![]()
где m — масса образовавшегося при электролизе i-вещества (г); Э — эквивалентная масса i-вещества (г/моль); М — молярная масса i-вещества (г/моль); n — заряд i-иона; I — сила тока (A); t — продолжительность процесса; F — константа Фарадея, характеризующая количество электричества, необходимое для выделения 1 эквивалентной массы вещества (F = 96 500 К = 26,8 А•ч).
Смотрите также
Ниобий
Ниобий — это химический
элемент XX в. в прямом и переносном смысле. Хотя как элемент его
открыли в самом начале XIX в. (1801 г.), но как металл был получен лишь
век спустя (1907 г.), а сейчас без н ...
Определение свойств газов
Общие сведения о свойствах
газов
В природе в
нормальных условиях (при комнатной температуре и атмосферном давлении)
сравнительно немногие химические вещества находятся в газообразном сос ...
Свойства краун-эфиров и фуллеренов
Нанотехнология
и наноматериалы наряду с биотехнологией, информационными технологиями являются
ключевыми технологиями 21 века. Это подтверждается и резким ростом
финансирования данной отрасл ...


