Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Билет №5. (углубленный)Статьи и работы по химии / Билеты по химии 10 класс / Статьи и работы по химии / Билеты по химии 10 класс / Билет №5. (углубленный) Билет №5. (углубленный)Страница 1
Электролиты и неэлектролиты. Электролическая диссоциация неорганических кислот, солей, щелочей. Степень диссоциации.
Электролит проводит электрический ток в результате того, что направленное перемещение его ионов создает поток электрических зарядов. Таким образом, пропускание электрического тока через электролит сопровождается переносом вещества.
Электролитами чаще всего являются такие соединения, как кислоты, основания или соли, находящиеся в расплавленном состоянии или в водных растворах. Способность электролитов проводить электрический ток называется электролитической проводимостью. Ее следует отличать от электронной проводимости обычных проводников электрического тока, например металлов. В веществах с электронной проводимостью поток заряда обусловлен потоком электронов, а не перемещением ионов. Поэтому пропускание электрического тока через проводники с электронной проводимостью не сопровождается переносом вещества.
Электролиты в свою очередь могут быть подразделены на два типа: сильные и слабые электролиты. Сильный электролит – это соединение, которое в расплавленном состоянии или в растворе полностью ионизировано. Примером сильного электролита может служить соляная кислота. При растворении хлороводорода в воде происходит его полная ионизация:
![]()
В этом уравнении использована простая (а не двойная) стрелка, чтобы показать, что процесс идет в указанную сторону до полного завершения.
Слабый электролит – это вещество, которое диссоциирует на ионы лишь частично. Следовательно, в растворе устанавливается равновесие между недиссоциированными молекулами такого вещества и диссоциированными ионами. Примером слабого электролита является уксусная кислота:
![]()
Органические кислоты и основания обычно являются слабыми электролитами.
Неэлектролит вообще не диссоциирует на ионы и поэтому не обладает способностью проводить электрический ток. Большинство органических соединений принадлежат к неэлектролитам.
Механизм электролитической диссоциации — распада молекул или кристаллов растворяемого вещества на ионы под влиянием молекул растворителя — был понят несколько позднее. Согласно современным воззрениям, такой распад является результатом взаимодействия полярных молекул растворителя, например воды, с молекулами или кристаллической решеткой растворяемого вещества. Молекулы растворителя атакуют кристаллическую решетку, разрушая ее и переводя составные части решетки (ионы) в раствор в форме сольватированных (гидратированных) заряженных частиц Окружающие эти ионы полярные молекулы растворителя ориентированы в соответствии с зарядом ионов. Растворение электролита в известной мере упорядочивает молекулы растворителя. Естественно предположить, что эта способность к упорядочению молекул растворителя у многозарядных ионов выражена сильнее, чем у однозарядных. В этом и нужно искать причину того, что соли, содержащие многозарядные ионы, плохо растворимы (в ряде случаев практически нерастворимы) в воде. Например, хлорид бария растворим хорошо, а сульфат бария — очень плохо. Следовательно, влияние растворенного вещества и растворителя является обоюдным: полярные молекулы растворителя разрушают кристаллическую решетку растворяемого вещества на отдельные ионы, а эти ионы, переходя в раствор, вызывают изменение растворителя, заставляя его молекулы упорядочиваться. Кроме того, сольватированные ионы растворенного вещества не индифферентны по отношению друг к другу. Противоположно заряженные ионы имеют тенденцию притягиваться силами электростатического взаимодействия, образуя нейтральные молекулы или нейтральные группы молекул. Разумеется, в реальном растворе всегда присутствуют как отдельные сольватированные ионы, так и нейтральные молекулы.
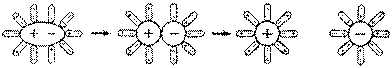
Действие растворителя на растворенное вещество настолько велико, что может вызывать электролитическую диссоциацию веществ, не обладающих ионным типом связи. Например, полярные молекулы хлороводорода, растворяясь в воде, разрываются ее молекулами на ионы. При растворении хлороводорода в бензоле, являющемся менее полярным растворителем, чем вода, диссоциации молекул не происходит. Поэтому раствор хлороводорода (кислота) в воде проводит электрический ток, а в бензоле нет.
Смотрите также
Ионоселективные электроды
Для определения состава и свойств различных
соединений и растворов используются химические, физические и физико-химические
методы анализа. В некоторых случаях появляется необходимость опреде ...


